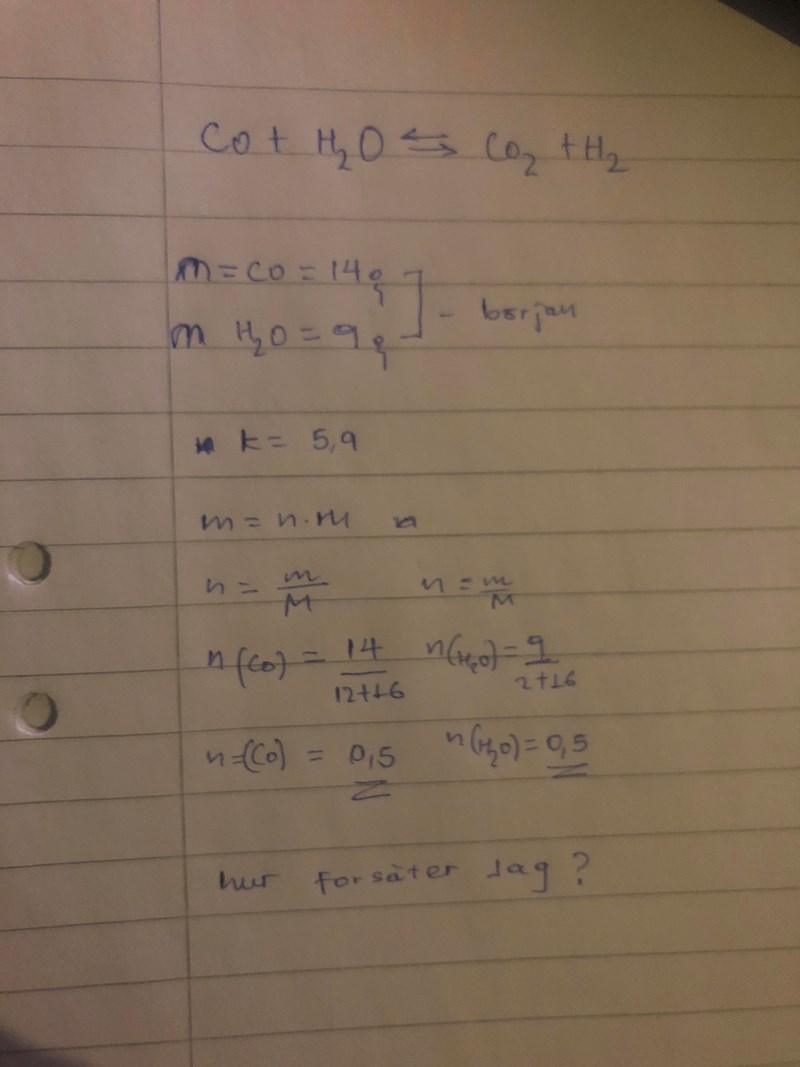jämvikt
Jag förstår inte den här fråga ur syntes kemi två Anders Henrikson 
Välkommen till Pluggakuten!
Hur har du tänkt själv? Det står i Pluggakutens regler att du skall visa hur du har försökt och hur långt du har kommit. /moderator
Eftersom du har lika många mol gas totalt på båda sidor kan du räkna med substansmängder i stället för koncentrationer.
Antag att x mol koldioxid reaglerar. Hur mycket finns det av varje ämne vid jämvikt?
Anta att x mol CO reagerar med x mol vatten. Hur många mol vätgas respektive kolmonoxid bildas? Hur många mol finns kvar av CO respektive vatten?
- jag fick X1 = 0,8449
- och X2 = 0,355
- det står i facit att det blir 16 g eller 0,354 men hur blir det 16g
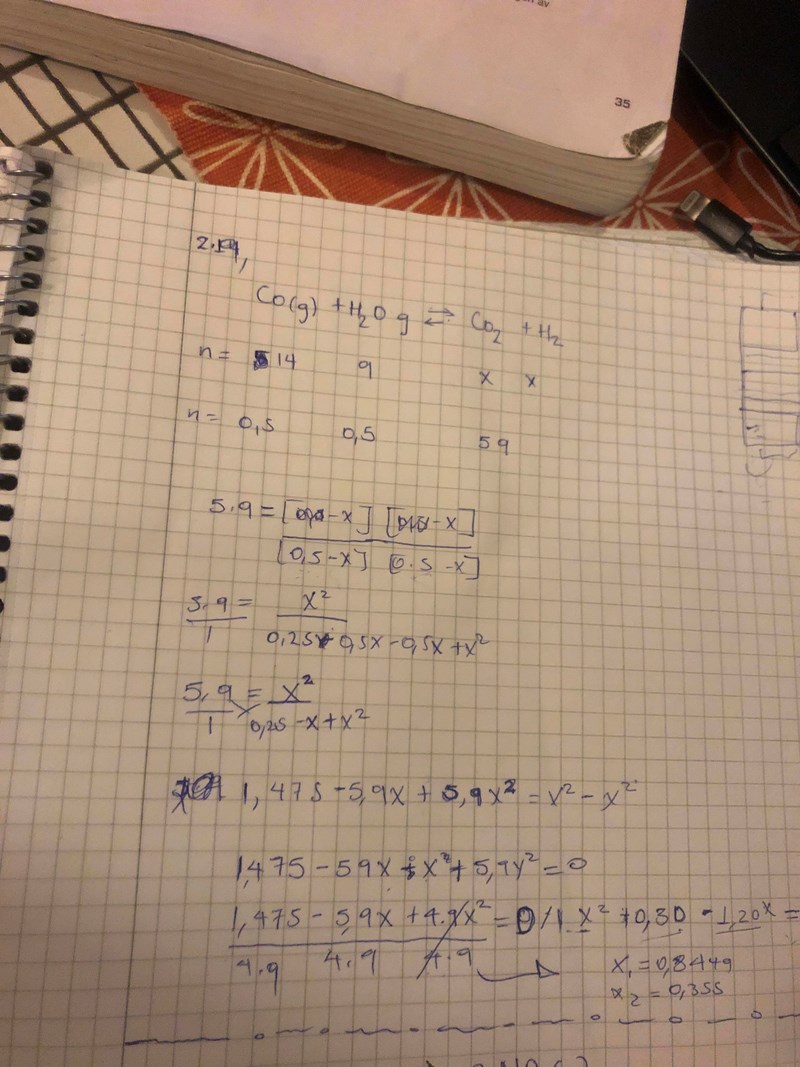
Nej, du utgår från en blandning som bara innehåller kolmonoxid och vatten, d v s substansmängderna för koldioxid och vätgas är 0 före jämvikt. Du har skrivit något annat på första raden, men på andra raden står det x2, som det borde. Du har alltså jämviktsekvationen . Dra roten ur båda sidor och fortsätt därifrån.