Polytropsamband
Hej.
Jag förstår inte riktigt hur man tänker när man gör denna omskrivningen vid ett polytropsamband. Sambandet är . T = temperatur, V = volym och n = polytropexponenten (som i detta fall är = 1,4). Detta förstår jag, men det är nu, när man skriver om volymkvoten som jag inte hänger med. Det gäller en idial dieselcykel.
. Detta hänger jag inte riktigt med på.
Vad är ?
Här skrev jag ett helt felaktigt inlägg, som jag nu har ändrat ett par gånger. Så här skall det vara:
Första bråket i ditt högerled borde vara inverterat. Parentesen borde bara stå om volymbråket.
Så här borde ekvationen se ut:
Detta är cykeln:
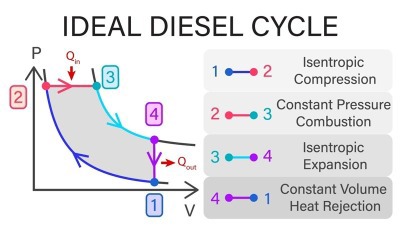
Vi har polytrop expansion (egentligen isentrop i den ideala cykeln) mellan 3 och 4:
Vi vet ofta kompressionsförhållandet mellan och varför vi vill göra omskrivningen från till . Då du har en ideal gas som genomgår en isobar process mellan 2 och 3 () får vi:
Alltså:
Detta ger:
V.S.V
Bubo skrev:
Här skrev jag ett helt felaktigt inlägg, som jag nu har ändrat ett par gånger.
Tryckfelsnisse verkar varit framme igen, ser jag.
Jag räknade på två stycken isentropiska processer. Totalt fel.


