Adiabatisk process: Temperatur i läge 2.
Uppgift: Koldioxidgasen (1,08 mol) har i läge 1 temperaturen 26,03 °C och trycket 1,13 bar. Gasen expanderar utan värmeutbyte med omgivningen till läge 2, där trycket är p2. Därefter, vid konstant volym, ökar trycket tills den åter når temperaturen 26,03 °C i läge 3.
Om volymen i läge 2 är 26,3 ·10-3 m³, vad är då temperaturen i läge 2? Ange svaret i grader celsius.
Jag antog korrekt att det var en adiabatisk process, så jag antog även att jag kunde beräkna temperaturen i läge 2 med hjälp av allmänna gaslagen () och poisson's lag (). Mitt svar blev 14,2 grader celsius men det korrekta svaret var 17,1 grader celsius.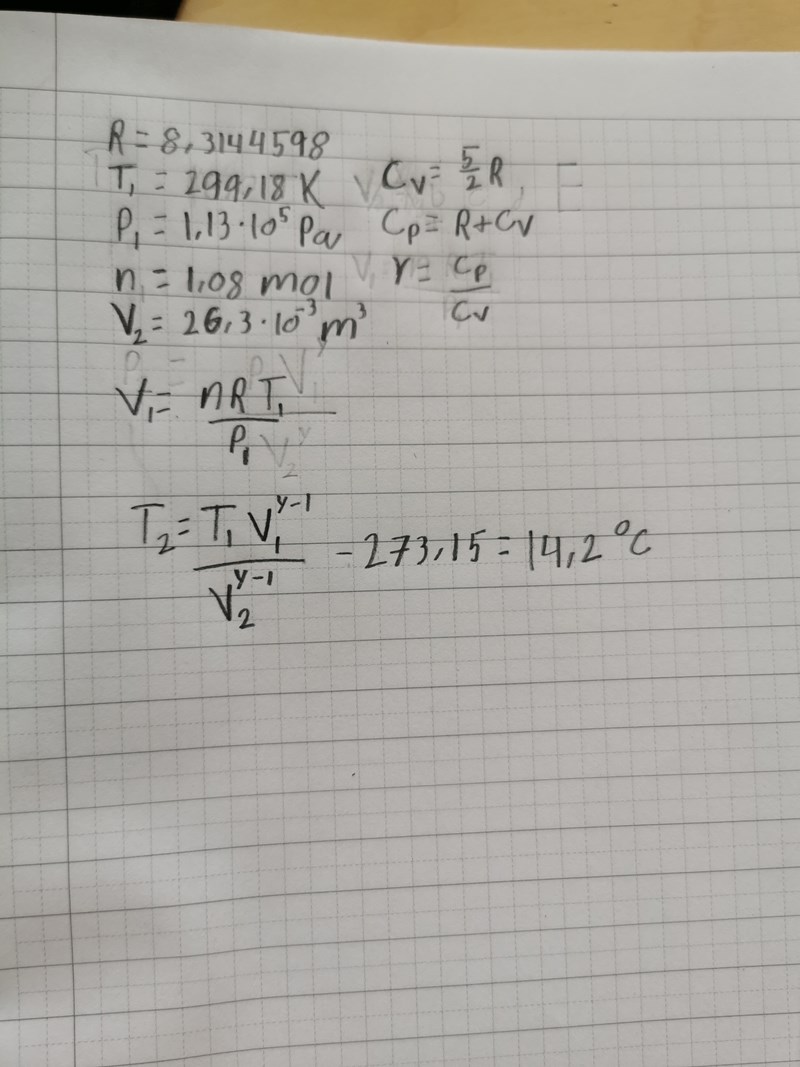
Edit: Det är tydligt att ditt adiabatiska index är problemet. Ditt antagande kring specifika värmekapaciteterna och är alldeles för grovt.
Du får 17.1 om du inte avrundar beräknade volymen .
@Ebola
Hur fick du gamma till att bli 1,3? Jag får det alltid till 1,4 för diatomära gaser.
P.S. Det skulle vara 17.1 grader, inte 17,2. Jag skrev fel.
Om du kollar upp adiabatiskt index för koldioxid vid rumstemperatur får du .
Om du härleder adiabatiskt index för polyatomära (tre eller fler) ideala gaser får du .
Vilken du ska använda framkommer sannolikt ur boken uppgiften är hämtad eller föreläsningar som du haft tillgång till.
Du kan använda båda men bör motivera och ange varför du gör antagandet. Anledningen till att den du använder inte är särskilt lämplig här är för att gäller för diatomära ideala gaser.
Tack, då förstår jag.


