Amfolyters PH-värde
Hej!
Jag undrar om alla amfolyter har PH-värde 7 liksom vatten, H2O har, eftersom att de både kan vara en syra och en bas (och jag tror att amfolyter även har lika hög koncentration av oxoniumjoner och hydroxidjoner)?
Tack på förhand!
Jag tror att avjoniserat vatten har det exakta pH värdet 7 däremot vanligt vatten skulle ligga jätte nära 7 och inte exakt på 7 pga de andra jonerna som finns i vanligt vatten
Ja, men det var inte riktigt det jag undrade. Jag undrar om alla amfolyter har PH-värdet 7 eller varierar amfolyternas PH-värden?
Amfolyter har inte något särskilt pH-värde, men det är stor skillnad på pH-värdet då amfolyten HSO4- dominerar jämfört med H2SO4 och SO42- och det pH-värde då amfolyten HPO42- dominerar över H2PO4- och PO43-.
Är det svar på din fråga?
Okej, så om jag har förstått det rätt så kan alla amfolyter ha olika pH-värden, amfolyterna har alltså inge bestämt pH-värde utan skiljer sig åt amfolyt till amfolyt? Sen så undrar jag också om du menar att vissa amfolyters pH värde kan variera beroende på vilka andra ämnen de reagerar med, stämmer detta?
När man pratar om pH-värde, så handlar det alltid om vattenlösningar. Vilket pH en vattenlösning har beror dels på vilka ämnen som är upplösta i vattnet, dels dessa ämnens koncentrationer.
Smaragdalena skrev:När man pratar om pH-värde, så handlar det alltid om vattenlösningar.
Jaha det visste jag inte! Så ett rent ämne i sig har alltså inte något eget pH-värde? Jag trodde nämligen t.ex. att saltsyra alltid har pH-värdet 0/1 och att natriumhydroxid alltid har pH-värdet 14 utan att behöva vara upplösta i vatten.
Då hade du fel. Tänk på hur definitionen av pH-värde ser ut! Dessutom är det fullt möjligt att ha pH-värden som är mindre än 0 eller större än 14.
Men då betyder det väll att ett ämnes pH-värde kan variera beroende på hur stor koncentration det finns av ämnet i vattenlösningen, eller hur? Om det nu skulle vara så att pH-värde varierar beroende på dess koncentration, hur kommer det då sig att det ändå finns bestämda pH-värden på vissa ämnen som du t.ex. kan se nedan?
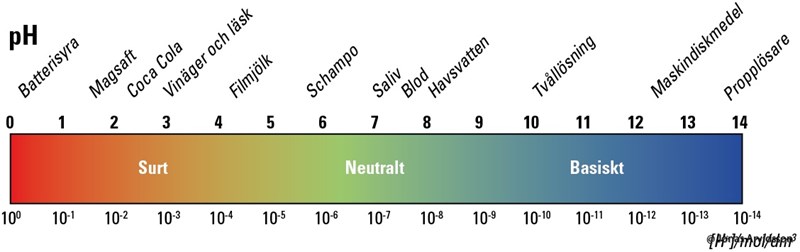
Det finns en viss (ungefärlig) koncentration av svavelsyra i batterisyra. Det finns en viss (ungefärlig)koncentration av saltsyra i magsaft. Det finns en viss koncentration av fosforsyra och kolsyra i cocacola. Det finns en viss koncentration av ättiksyra i vinäger. och så vidare, och så vidare, och så vidare...
Smaragdalena skrev:Det finns en viss (ungefärlig) koncentration av svavelsyra i batterisyra. Det finns en viss (ungefärlig)koncentration av saltsyra i magsaft. Det finns en viss koncentration av fosforsyra och kolsyra i cocacola. Det finns en viss koncentration av ättiksyra i vinäger. och så vidare, och så vidare, och så vidare...
Ja men är de fortfarande upplösta i vatten då?
Ja, i samtliga fall. Det borde ha stått "maskindiskmedel, brukslösning" och "propplösare, brukslösning" eller något liknande, men det var väl så självklart för den som gjorde tabellen att man inte tänkte på det.
Okej, men kan pH värdet för dessa ämnen variera mycket eller endast lite beroende på hur hög koncentrationen av ämnet är?
Om du tar t ex en 33 dl burk cocacola och blandar drickan med 1 liter vatten, så kan man knappast kalla det cocacola längre, eller hur? Så pH-värdet för cocacola kan inte variera särskilt mycket.
Om du tar 1 dl propplösar-blandning, häller det i en 10-litershink och späder det tills hinken är full kommer du att få en lösning med pH = 12 om pH var 14 från början (och propplösare är ren NaOH,som jag tror).
Okej! Men när man gör pH-skalan (som t.ex. den på bilden) hur stor mängd vatten utgår man ifrån då?
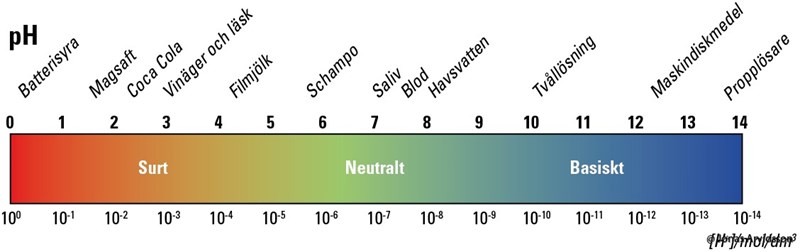
Hur mycket vatten det är spelar ingen roll, det är koncentrationerna som är intressanta.
Okej, men vilken koncentration har man utgått ifrån på bilden ovan?
För batterisyra, magsaft, cocacola, vinäger, läsk, filmjölk, schampoo, saliv, blod och havsvatten är det väl ganska klart att man har valt de koncentrationer som batterisyra, magsaft, cocacola och så vidare har "naturligt", När det gäller tvållösning, maskindiskmedel och propplösare skulle jag gissa att man har mätt på de lösningar som det blir när man använder ämnena "normalt".



