Aminosyror - Förändringar i pH
Hej! Det är en fråga jag fortfarande funderar över, trots flera förklaringar.
Jag fick höra att i ett fall är det R-gruppen (om den innehåller en karboxyl- eller amingrupp) som tar upp eller släpper ifrån sig protoner vid pH-förändringar. Detta gör att den blir neutral och därmed inte längre kan attrahera motsatt laddning, vilket leder till att proteinet vecklas upp och förstörs.
Men i ett annat sammanhang diskuterade vi att det INTE är sidokedjan (R-gruppen), utan snarare aminosyrans egna karboxyl- och amingrupp, som agerar som syror och baser vid pH förändringar. Jag förstår inte riktigt vad som händer när, och om det jag pratar om stämmer. Uppskattar hjälp med att förtydliga detta.
Anteckningar från ett sammanhang där själva aminosyrans karboxyl och amingrupp reagerar som syra/bas:
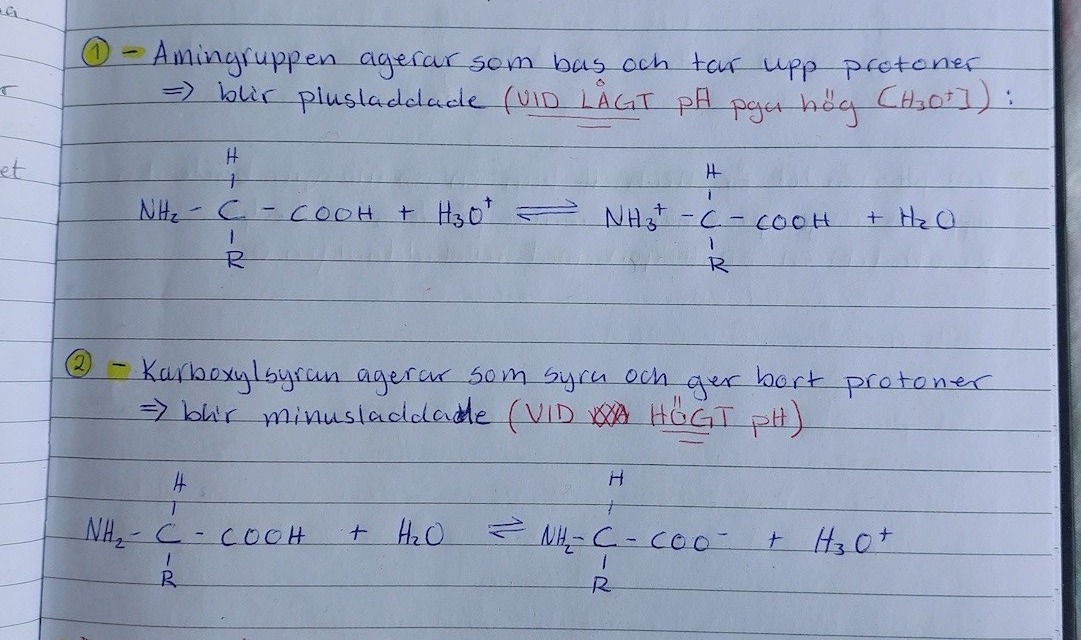
Dr.scofield skrev:Hej! Det är en fråga jag fortfarande funderar över, trots flera förklaringar.
Jag fick höra att i ett fall är det R-gruppen (om den innehåller en karboxyl- eller amingrupp) som tar upp eller släpper ifrån sig protoner vid pH-förändringar. Detta gör att den blir neutral och därmed inte längre kan attrahera motsatt laddning, vilket leder till att proteinet vecklas upp och förstörs.
Ja det är en av flera förändringar som kan leda till att ett proteins struktur förändras (t.ex. genom att "vecklas upp" en del som du skrev), och det kan leda till att proteinet denatureras och "förstörs".
Men i ett annat sammanhang diskuterade vi att det INTE är sidokedjan (R-gruppen), utan snarare aminosyrans egna karboxyl- och amingrupp, som agerar som syror och baser vid pH förändringar. Jag förstår inte riktigt vad som händer när, och om det jag pratar om stämmer. Uppskattar hjälp med att förtydliga detta.
Ja, men detta stämmer för enskilda aminosyror, och i ett protein de två ändarna av polypeptiden. Men om du tittar på peptidbindningen, så ser du att karboxyl- eller aminogruppen kar kombinerats och bildar istället peptidbindningen.
Det är m.a.o. skillnad mellan de fria aminosyrorna, och när de binder till varandra med peptidbindningen.
Det första angående R gruppen stämmer alltså bara om den innehåller en egen karboxylgrupp eller amingrupp? (Bortsett från vad R gruppen består av)
Angående detta med enskilda aminosyror har jag blivit tillsagd att det snarare har med pI att göra, och det är då som det jag skrev i bilden händer. Hade du kunnat vara snäll och förklarat sammanhanget mellan dem två?
Dr.scofield skrev:Det första angående R gruppen stämmer alltså bara om den innehåller en egen karboxylgrupp eller amingrupp? (Bortsett från vad R gruppen består av)
Angående detta med enskilda aminosyror har jag blivit tillsagd att det snarare har med pI att göra, och det är då som det jag skrev i bilden händer. Hade du kunnat vara snäll och förklarat sammanhanget mellan dem två?
Ta en titt i kemiboken för reaktionen där peptidbindningen bildas (eller leta fram en bild på nätet), så kommer du se att det inte är en amino- eller karboxylgrupp längre. Det är en annan funktionell grupp - som inte tar upp eller lämnar ifrån sig protoner på samma vis.
Här har jag ett exempel. OH gruppen i ena aminosyrans karboxylgrupp reagerar med vätet i andra aminosyrans aminogrupp och bildar vatten. Resten går ihop via kondensationsreaktion och binder med peptidbindning.
Men vad har detta med frågan att göra? 😅

Ja precis, där ser du att i polypeptiden förenas aminosyraresterna med varandra genom peptidbindningen. Och i din bilds polypeptid, finns det endast en aminoände (vänster) och en karboxylgrupp (höger).
Dessa ändar kan agera som syra/bas, precis som arginins sidokedja. Alla grupper som kan agera som syra eller bas kommer påverkas av pH, och laddningen förändras.
Och ett protein som består av massvis med aminosyrarester, kommer det finnas många fler sidokedjor med funktionella grupper, jämfört med de två ändarna - därför har sidokedjornas laddning en större effekt (genom att de är fler).
Alla grupper som kan agera som syra/bas kommer påverkas av pH, och alla dessa grupper kommer påverka proteinets struktur.
Tack så mycket för hjälpen! Jag börjar förstå helheten i detta nu.
Grejen är att vi nu har nämnt vad som händer vid pH-ändringar med
- R-gruppen
- aminosyrans karboxyl- och aminogrupp, samt
- C- och N-terminalerna.
Skulle uppskatta det mycket om du kunde sammanfatta kort vad som händer med varje del, så att jag kan anteckna ner skillnaden mellan dem och öva inför provet i biokemi. Tackar dig återigen!


