Balansering med hjälp av oxidationstalsmetoden
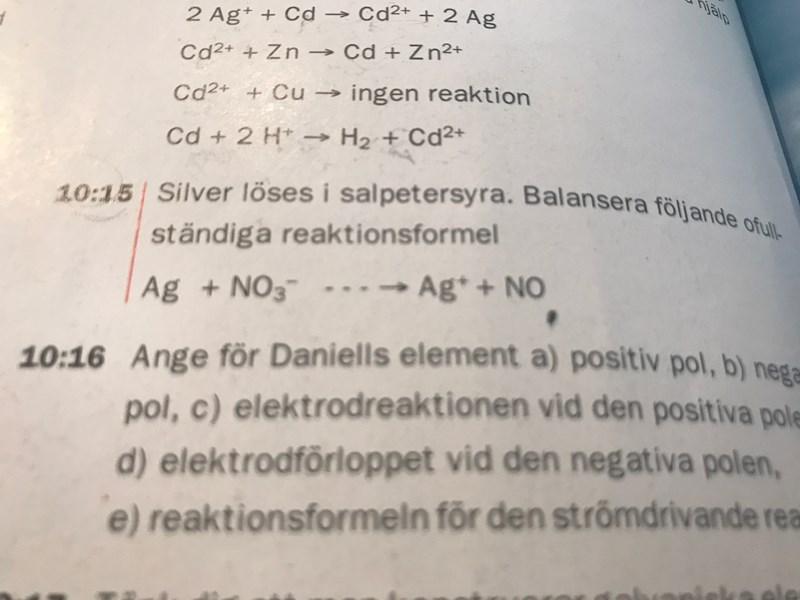 Hej!
Hej!
(10:15)
Jag har försökt balansera denna reaktion men jag får inte till det, väte ska också finnas med i reaktionen och det bildas även vatten. Varför blir silver plusladdad?
Därför att silver bildar envärt positiva joner - att det är så, är det bara att acceptera och lära sig. (Det är så ologiskt att koppar, silver och guld, som finns i samma grupp i periodiska systemet och altså "borde" bete sig likadant kemiskt sett, har som vilktigaste jonladdning +2, +1 respektive +3.)
Det är alltså silver som oxideras ett steg till silverjon. Det är kväveatomen i nitratjonen som reduceras. Vilket ox.tal har kväve i nitratjonen? Vilket ox.tal har kväve i kväveoxid? Hur många steg har kvävet reducerats? Kom sedan tillbaka om du behöver hjälp med resten.
Hur vet du att det är kvävet som reduceras?
Jag fick 3Ag + NO3 3Ag+ + No
hur många väte ska det vara?
Eftersom syre för det mesta behåller sitt oxidationstal -II i sina föreningar.
Vilket oxidatiostal har kväve i nitratjonen respektive i kväveoxid? Det behöver du redovisa om du skall ge en fullständig lösning på den här uppgiften.
Det kommer att bildas lika många kväveoxidmolekyler som det fanns nitratjoner från början. De syren som blir över kommer att bli till vatten. Hur många vattenmolekyler kommer det att bildas? Hur många väte kommer det att behövas till de vattenmolekylera? (Reaktionen sker i sur miljö, så det kommer att finnas gott om oxoniumjoner tillgängliga. Eftersom man är lat skriver man bara i stället för hela oxoniumjonen - dessutom blir det mindre rörigt om man slipper de extra vattenmolekylerna på högersidan.)


