Beräkna fosforsyrans koncentration i den dryck du titrerat.
 Hej!
Hej!
Jag hade labborerat kring bestämning av koncentrationen fosforsyra i Coca Cola. Väldigt intressant laboration.
Iallafall jag hade fått material:
 Jag kommer helt enkelt att beräkna fosforsyrans koncentration vid den första ekvivalentpunketen.
Jag kommer helt enkelt att beräkna fosforsyrans koncentration vid den första ekvivalentpunketen.
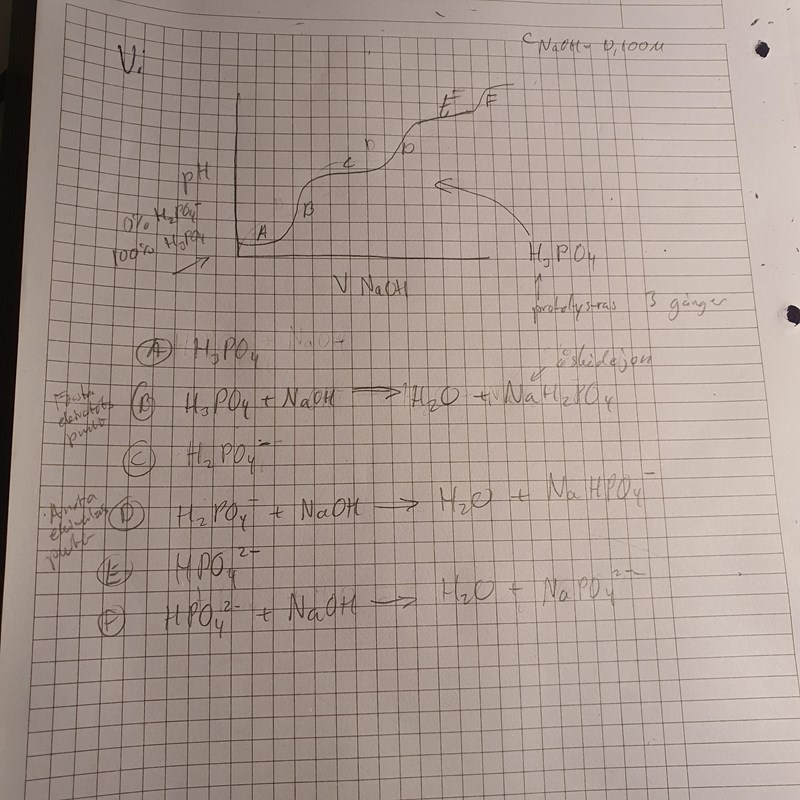
Med det gjorde jag min tilteringskurva där jag kan använda för att få fram pH värdet och Ka. Osv.

Jag tror att jag har överkomplicerat med att få fram vad koncentrationen fosforsyra är. Jag fick fram till att X = 0,0141835599M vilket jag är osäker. Ville bara veta om det jag gör är rätt.
Kan du lägga in dina bilder på rätt håll? Nu känner jag mig så här: 
Smaragdalena skrev:Kan du lägga in dina bilder på rätt håll? Nu känner jag mig så här:
Ber om ursäkt. Jag ville bara fråga om jag har rätt kring fråga 2 a) där den säger att med hjälp av den andra ekvivalentpunketen kan du räkna ut Coca colans halt av kolsyra dvs löst koldioxid
Vilken partikelslag reagerar med hydroxidjonerna mellan första och andra ekvivalentpunketen? Skriv formler för reaktionerna.
Jag skrev H3PO4 (aq) + NaOH (aq) → H2O + NaH2PO4 (aq)
Men jag förstår inte vilken partikelslag som reagerar med hydroxidjonerna
Det du har skrivit är första ekvivalenspunkten, inte andra. Divätefosfatjonen är också en syra, som kan reagera med ytterligare en hydroxidjon. (Väteforsfatjonen är också en syra, men den år så svag att man inte kan åstadkomma en tillräckligt basisk vattenlösning att man kan få den att reagera med hydroxidjoner.)
Smaragdalena skrev:Det du har skrivit är första ekvivalenspunkten, inte andra. Divätefosfatjonen är också en syra, som kan reagera med ytterligare en hydroxidjon. (Väteforsfatjonen är också en syra, men den år så svag att man inte kan åstadkomma en tillräckligt basisk vattenlösning att man kan få den att reagera med hydroxidjoner.)
Så vad som händer att vid första ekvivalentpunketen så reagerar Divätesfosfat med natriumhydroxid och därefter blir kvar vätefosfatjoner kvar. Vid den andra ekvivalentpunketen så blir det den korresppnderande "bas" till H2PO3
HPO4^2- + H20 -><- PO4^3- + OH-
Jag tror jag förstår inte riktigt. Det säger att man ska skriva ner FORMLER. Alltså det finns flera än 1.
Nej, nu har du skrivit vad som händer vid det tredje steget. Det är det andra steget du borde skriva.
Smaragdalena skrev:Nej, nu har du skrivit vad som händer vid det tredje steget. Det är det andra steget du borde skriva.
Okej, så först så är den korresppnderande basen till H2PO4- är HPO4^2-
Formlen kommer att bli
HPO4^2- + H2O -><- H2PO4- + OH-
Så vi får en baskisk neutralisation där partikelslagen är H2PO4- som reagerar med OH-.
Frågar lyder till att det finns fler än 1 partikelslag som reagerar med OH- mellan första och andra ekvivalentpunketen
Alltså det finns en annan formel till?
Nej, divätefosfatjonen är (även) en syra.
Det finns två partikelslag som reaglerar med hydroxidjonerna: forsforsyra och divätefosfatjon. När man har tillsatt lagom mycket hydroxidjoner för att de skall kunna reagera med alla fosforsyra-molekyler har man nåt den första ekvivalenspunkten. När man har tillsatt lika mycket hydroxidjoner till, så att de har reagerat dels med forsforsyra-molekylern aoch dels med divätefosfatjonerna, har man kommit till den andra ekvivalenspunkten.
Smaragdalena skrev:Nej, divätefosfatjonen är (även) en syra.
Det finns två partikelslag som reaglerar med hydroxidjonerna: forsforsyra och divätefosfatjon. När man har tillsatt lagom mycket hydroxidjoner för att de skall kunna reagera med alla fosforsyra-molekyler har man nåt den första ekvivalenspunkten. När man har tillsatt lika mycket hydroxidjoner till, så att de har reagerat dels med forsforsyra-molekylern aoch dels med divätefosfatjonerna, har man kommit till den andra ekvivalenspunkten.
 okej, jag tror att det klickar i huvudet.
okej, jag tror att det klickar i huvudet.
Om jag har uppfattat det rätt så är det:
(Första ekvivalentpunketen)
H3PO4 +NaOH-> H2O + NaH2PO4
Na är en åskådarjon som kan försummas.
(Andra ekvivalentpunketen)
H2PO4- + NaOH -> H2O + NaHPO4-
Partikelslag som reagerar med hydroxidjonen i första ekvivalentpunketen är fosforsyra. Partikelslag som reagerar med hydroxidjonen i andra ekvivalentpunketen är divätefosfatjonen.
Kan man försumma bort Na för både reaktionerna eftersom dem är bara åskådarjoner?
Kan man försumma bort Na för både reaktionerna eftersom dem är bara åskådarjoner?
Ja.
Smaragdalena skrev:Kan man försumma bort Na för både reaktionerna eftersom dem är bara åskådarjoner?
Ja.
Tack för hjälpen!
När man ska räkna ut löst koldioxid i detta försöket, och använder formeln
[CO2 (aq)] = (c(v2 - 2v1) )/V
Är då stora V volymen Coca-Cola som använts vid försöket?
ezez skrev:När man ska räkna ut löst koldioxid i detta försöket, och använder formeln
[CO2 (aq)] = (c(v2 - 2v1) )/V
Är då stora V volymen Coca-Cola som använts vid försöket?
Gör en ny tråd där du visar hur långt DU har kommit, så är det lättare att ge dig bra hjälp. /moderator
ezez skrev:När man ska räkna ut löst koldioxid i detta försöket, och använder formeln
[CO2 (aq)] = (c(v2 - 2v1) )/V
Är då stora V volymen Coca-Cola som använts vid försöket?
Good morning


