Beräkna koncentration genom titrering
 Uppgift 6H19
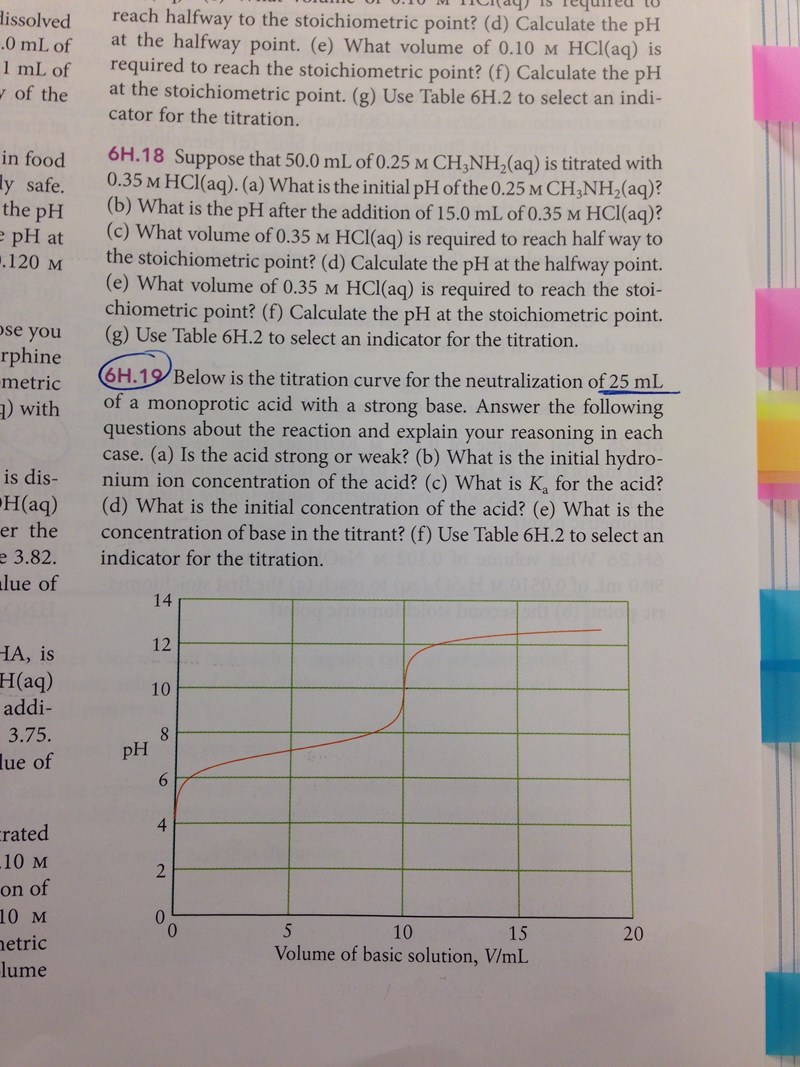
Uppgift 6H19
Jag vet att svaret p åa) blir svag syra, b) blir 10^-5 och c) blir 10^-7.5 = ca 3*10^-8
Men på d) vet jag inte hur jag ska ställa upp det.
Jag vet att jämviktskonstanter är för reaktion med substansen med vatten (1. eller?).
Så vi har att Ka(syran som blir titrerad) = 3*10^-8 är för reaktionen
HA + H2O <--> A- + H3O+
Men jag kommer inte längre än så.
där är syrans startkoncentration. Du kan göra antagandet att är ungefär lika stort som eftersom .
Är du säker på att svaret på b är 10^(-5)? Jag tycker det ser ut som pH 4 från början (men det är lite svårt att se).
SvanteR skrev :Är du säker på att svaret på b är 10^(-5)? Jag tycker det ser ut som pH 4 från början (men det är lite svårt att se).
Jo jag räknade med det också - men svaret blir rätt om man tar pH5 istället.
Samma sak när pH=pKa - tycker det ser ut som pH7 och inte minst när vi inte har siffror att räkna med så känns det konstigt de valt pH7.5 och avrundat svaret till 3*10^-8... men så är boken lite halvmissande (ganska många fel) och med märkliga saker som detta ;) Varför göra det lätt för nybörjar eleverna när man kan totalförvirra dem :P
Teraeagle skrev :där är syrans startkoncentration. Du kan göra antagandet att är ungefär lika stort som eftersom .
Tack!


