Bestämma det exakta pH-värdet för HAc
Hej!
Min uppgift är att bestämma pH-värdet för HAc innan en titrering utförts detta är vad jag kommit fram till:
Hittade denna formel för att kunna bestämma koncentrationen av oxoniumjoner för att sedan kunna räkna ut pH-värdet.
Ka=
I detta fall: Ka=
Räknar till en början därför ut syrakonstanten och sedan koncentrationen av HAc:
Ka för HAc:
pKa-värdet återfinns halvvägs till ekvivalenspunkten:
Den gröna punkten på grafen för HAc visar koordinaterna för pKa-värdet alltså vid pH= 4.89774 och vid V(NaOH) =9.749 *10⁻³ dm³, se diagram nedan.
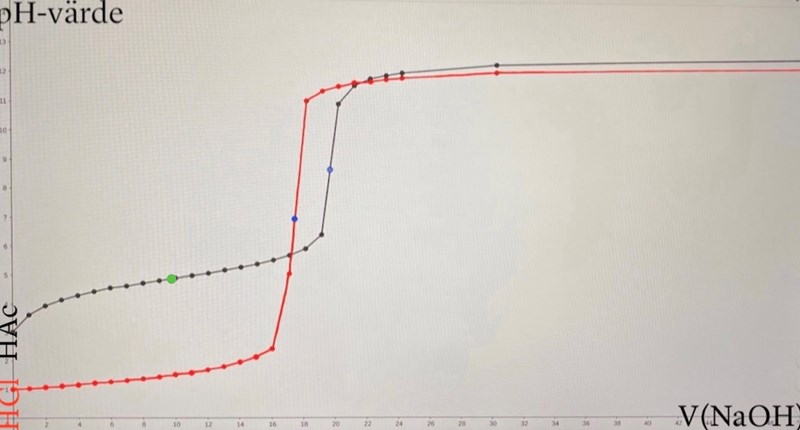
V(NaOH) vid halvtitrerpunkten = 19.498*10⁻³ dm³/2 = 9.749 *10⁻³ dm³
pH-värdet vid halvtitrerpunkten = 4.8974
Ka =
Då [HAc] = [Ac⁻] blir =1 → Ka = [H₃O⁺]
[H₃O⁺] = 10-4.8974 ≈ 1.226*10-5 mol/dm³
Ka- värdet för HAc är 1.8*10-5 mol/dm³ vid 25℃ enligt min lärobok, är mitt uträknade Ka- värde för HAc rimligt och rätt uträknat? Kan Ka-värdet för en svag syra skilja sig åt som jag i mitt fall fått fram?
Koncentration av HAc:
HAc (aq) + NaOH (aq) → NaAc (aq) + H₂O (l)
vilket leder till att 1 mol HAc (aq) ⇌ 1 mol NaOH(aq)
EP(HAc) ≈ 8.754 enligt diagrammet jag gjort
V(NaOH) ≈ 19.498*10⁻³ dm³ vid EP
n(HAc) = n(NaOH) = c*V = 0.100 mol/dm³*19.498*10⁻³ dm³ ≈ 1.9498*10⁻³ mol
c(HAc) =n(HAc)V(HAc)=1.9498*10⁻³ mol20.0*10⁻³ dm³ ≈ 0.09749 mol/dm³
Det exakta pH-värdet för HAc:
c(HAc) ≈ 0.09749 mol/dm³
Ka ≈ 1.226*10-5 mol/dm³
Ka=
1.266*10-5=
1.266*10-5(0.09749-x) = x2
x2+ 1.266*10-5x - 1.23422*10-6 = 0
x1=0.00111096 x2=- 0.00111096 svaret x2 förkastas då de är negativt
[H₃O⁺]= x1= 0.00111096 → pH = -lg(0.00111096) ≈ 3.954
Mitt uträknade pH-värde är 3.96 och pH-värdet jag fick innan titreringen börjades m.h.a. en pH-meter är pH-värdet = 3.01.
Hur kommer det sig att dom skiljer sig så mycket förutsatt att jag gjort min beräkningar rätt?
Bumpar min tråd då det gått 26 h utan svar :)

