Biokemi
 Hej jag behöver hjälp med en uppgift.
Hej jag behöver hjälp med en uppgift.
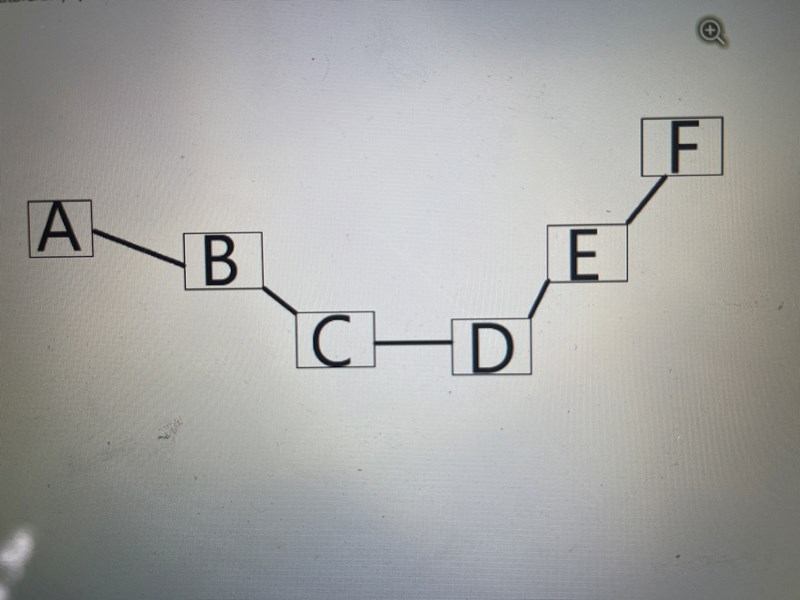
en denaturerad peptidkedja innehåller 6 aminosyror med olika kemiska egenskaper enligt figuren uppe. Aminosyra A och E har negativt laddade sidokedjor. Aminosyra B har elektropositiva atomer. Aminosyra C och F har hydrofoba sidoprojekt. Aminosyra D har många elektronegativa atomer.
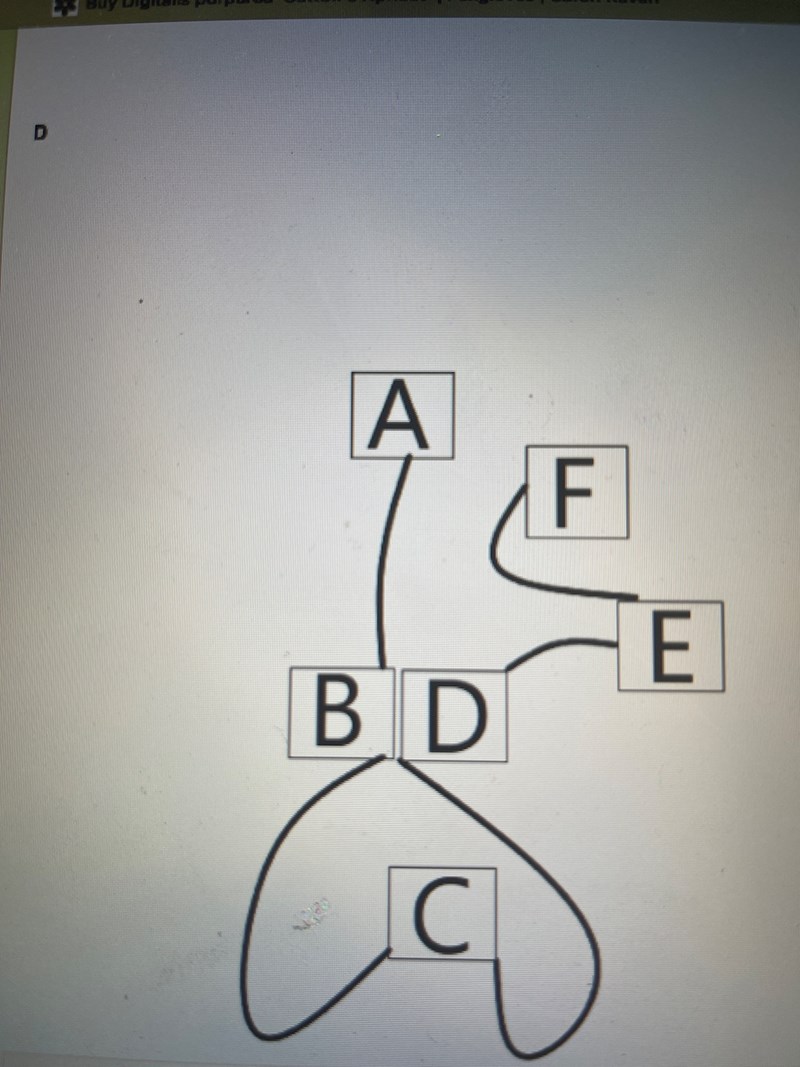
vilken av nedanstående konfigurationer (A,B,C, och D) kommer bli den mest stabila om peptiden renatureras och befinner sig i vattenlösning.


 Jag förstår inte hur jag ska tänka
Jag förstår inte hur jag ska tänka
I texten anges aminosyraresternas egenskaper. Du kan använda denna information för att lista ut svaret på två sätt, antingen:
1) så utgår du ifrån egenskaperna för att klura ut vilka som vill interagera med varandra. Som generellt i kemin, kommer negativa laddningar attrahera positiva. Polära kommer attrahera polära, och omvänt opolära kommer attrahera opolära.
2) eller så gör du antaganden om vilka funktionella grupper det är som döljer sig bakom t.ex. "negativt laddade sidokedjor". Det finns endast en funktionell grupp som vid neutralt pH är negativt laddad. Motsvarande kan göras för "elektropositiva atomer", för det finns endast en funktionell grupp som är elektropositiv vid neutralt pH (d.v.s. den har redan en positiv laddning). Om du listar ut vilka funktionella grupper som finns hos de respektive aminosyraresterna A-E, kan du para ihop dem med varandra (liknande i 1).

