Delokaliserade elektroner
I min kemi bok står det: "När en molekyl eller jon har flera närliggande atomer med fria elektronpar eller där atomerna är bundna med dubbelbindning kan resonansformler ge förståelse för elektronfördelning och därmed ämnets reaktivitet" Detta förstår jag inte.
Sådana formler kallas resonansformler:
Eller lite enklare:

En generell regel: ju fler resonansstrukturer man kan rita desto stabilare är ämnet.
Men för en acetatjon kan man rita följande resonansstrukturer:
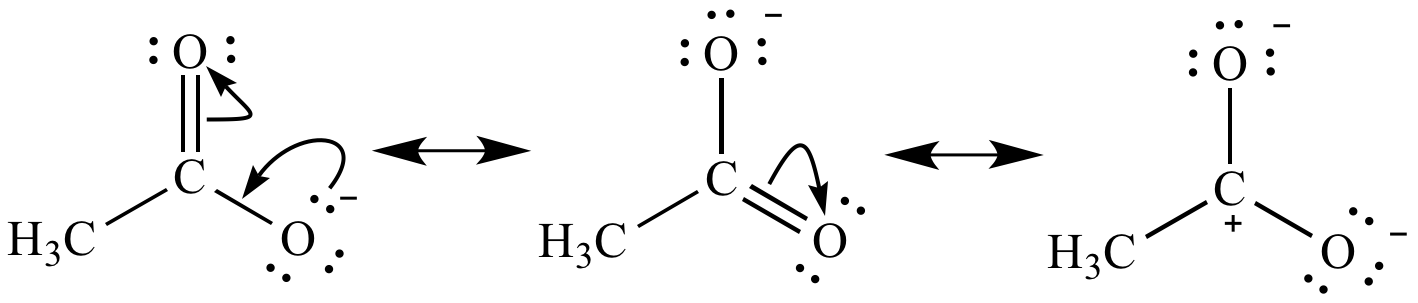
Här kan man tolka det så: vid neutralisering är sannolikheten att en vätejon binder sig till den negativt laddade syreatomen i strukturen till vänster lika med sannolikheten att vätejonen binder sig till den negativt laddade syreatomen i strukturen i mitten.

