Dipol
Är ammoniakmolekylen en dipol?
Kväve binder till 3 väte atomer.. Det är inte tydligt vart + och - laddningarna kommer hamna
Ja den är dipol
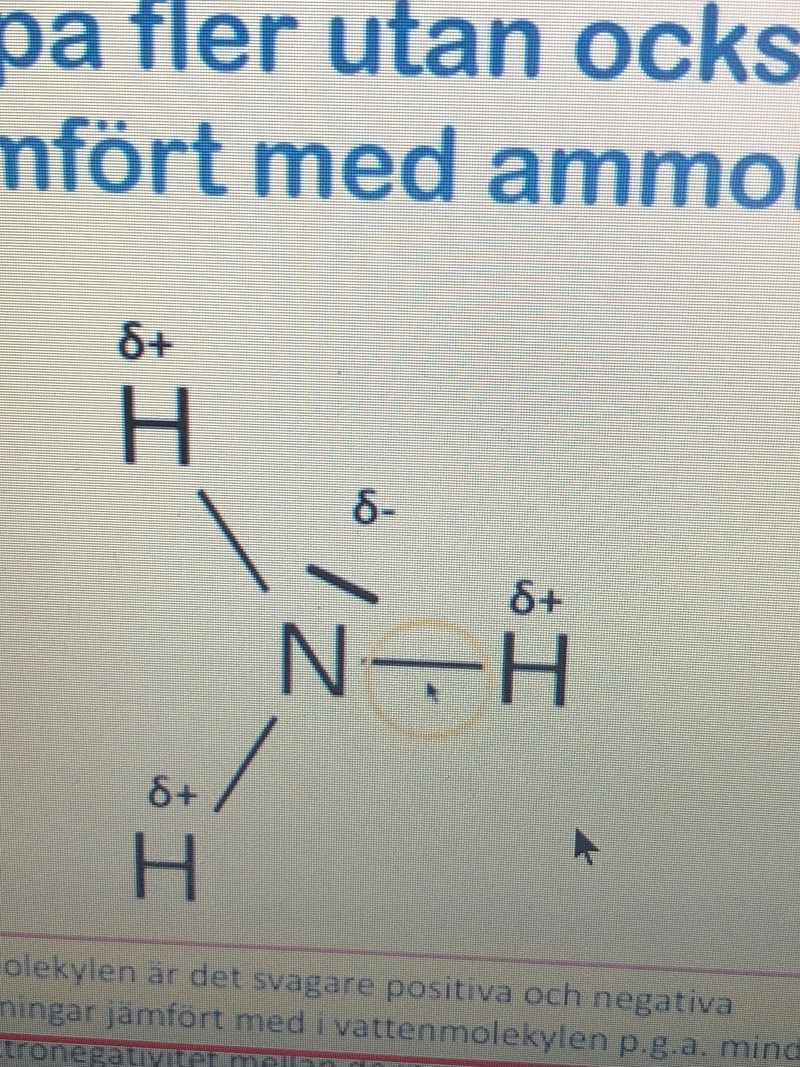
Så här ser en ammoniakmolekyl ut:  Kväveatomen, som är mer elektronegativ än väte (d v s är bättre på att dra till sig elektroner) är lite negativt laddad. Väteatomerna är lite positivt laddade. "Medelvärdet" för positiv laddning kommer att ligga mitt emellan de tre väteatomerna, strax under den lite negativt laddade kväveatomen.
Kväveatomen, som är mer elektronegativ än väte (d v s är bättre på att dra till sig elektroner) är lite negativt laddad. Väteatomerna är lite positivt laddade. "Medelvärdet" för positiv laddning kommer att ligga mitt emellan de tre väteatomerna, strax under den lite negativt laddade kväveatomen.
Men för att en molekyl ska vara en dipol måste den ju ha olika ”ben” dvs. Olika atomer som binder till varandra... Exempelvis propanol, där är molekylen vinklad ”har osymmetrisk form”. Kol binder till väte och ”OH” då har molekylen olika ”ben” , säger man ens ben? Finns det ett annat ord?
Men en ammoniak har ju 3 väte bundna till en kväve atom.. Alltså inte olika ”ben”. Men skillnaden i elektronegativiteten är stor, vilket leder till att de gemensamma elektroner förskjuts mer mot kväve, då får kväve partiell - laddning och syre + laddning... Men hur kan man annars avgöra om det är en dipol?
Men för att en molekyl ska vara en dipol måste den ju ha olika ”ben”
Varifrån har du fått den idén? Hur förklarar du i så fall att vatten är en polär molekyl?
Det jag menade är att man kan kolla på atomerna som ingår i molekylföreningen Bild 1: 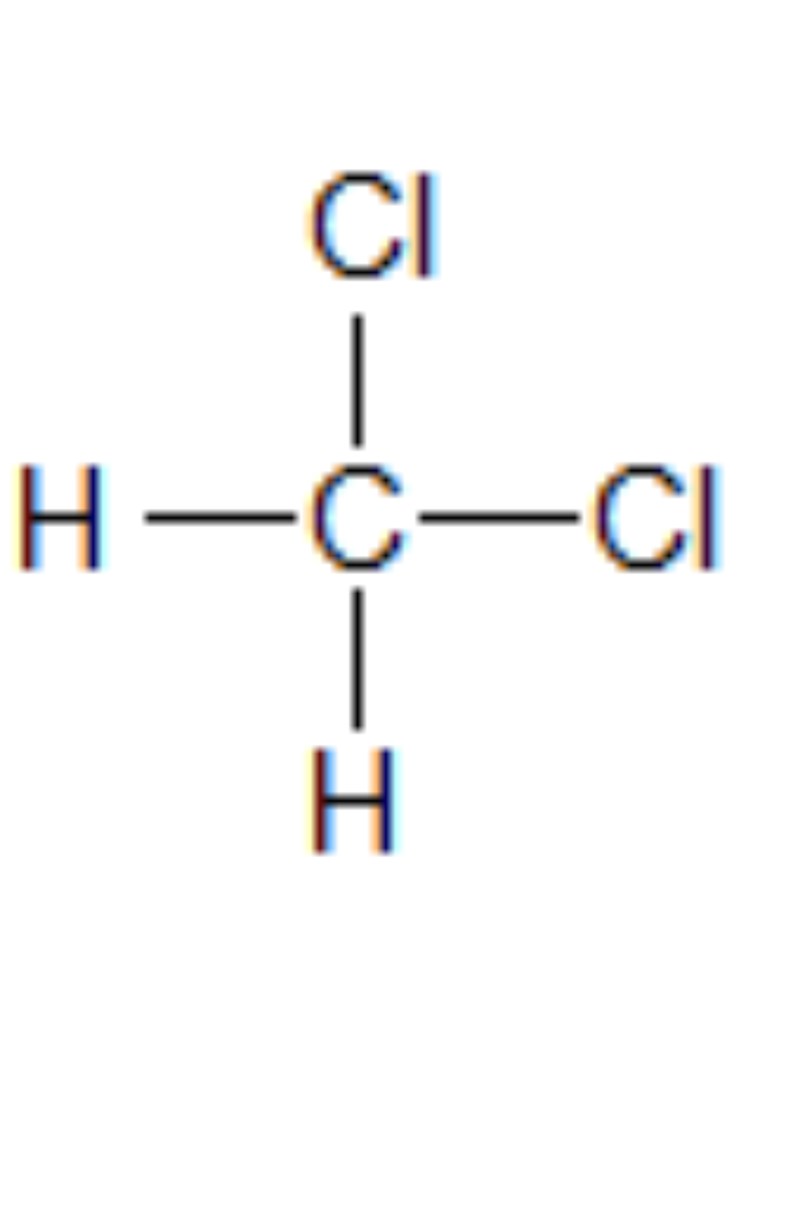
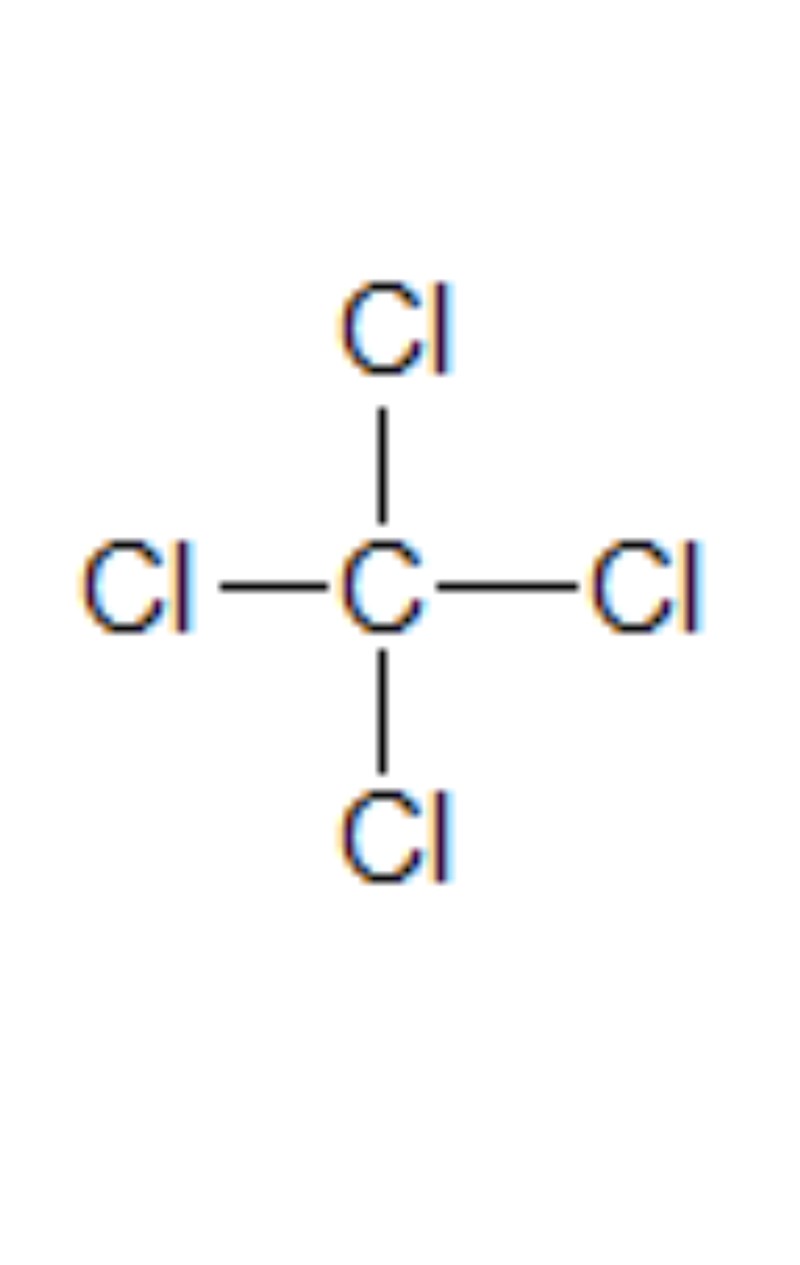 Bild 2
Bild 2
—-
Bild 1: Man kan tydligt se att det är polär kovalent bindning, alltså olika ämnen som sitter i samma molekyl, där den ena änden av molekylen blir + laddad och den andra änden - laddad
Bild 2 : Likadana ben , det är ingen dipol... + laddningen och - laddningen kommer hamna på samma ställe och ta ut varandra...
jag tror att ordet ben är fel att använda. Jag menar olika atomer som är bunda till varandra. För att en molekyl ska vara dipol måste det vara polär kovalent bindning. Det har inget att göra med ”ben”....
Läste du länken du fick i mitt förra inlägg?
Jag läste hela sidan
Min gissning är att du blandar ihop det med att en kolatom, som kan ha 4 enkelbindningar, måste binda till minst två olika sorters atomgrupper för att det skall kunna bli en dipol.


