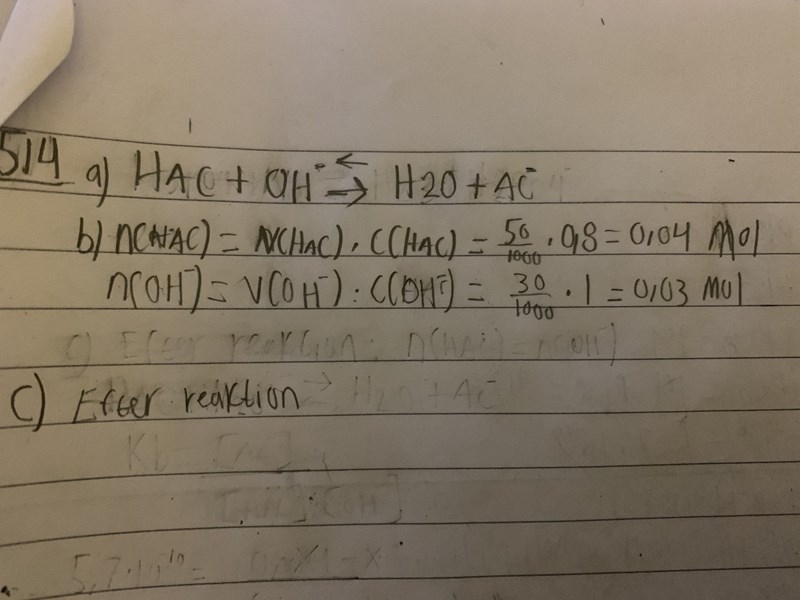Titrering av svag syra med stark bas
Detta är en fråga jag klurrat igenom men som jag ej fattar riktigt. Har inte riktigt fattat principen beräkningar av titrering. När ska man använda ICE och när är reaktionen reversibel?
Till 50,0 cm^3 ättiksyra med koncentrationen 0,80 mol/dm^3 sätter man 30,0 cm^3 natriumhydroxidlösning med koncentrationen 1 mol/dm^3.
A) Beräkna substansmängden HAc och HA- samt motsvarande koncentrationer efter reaktion.
Skulle någon vänligen kunna hjälpa mig med titrering av syror och baser?
Vad hade koncentrationen av ättiksyra respektive acetatjoner och hydroxidjoner varit i lösningen om ättiksyra var en stark syra?
Det här verkar vara första delen av en fråga. Kan du skriva av HELA frågan ord för ord, alternativt ta en bild och lägga upp här?
Hur många mol ättiksyra finns det i 50,0 cm3 ättiksyra med koncentrationen 0,80 mol/dm3? Hur många mol hydroxidjoner finns det i 30,0 cm3 natriumhydroxidlösning med koncentrationen 1 mol/dm3?
Ändrade rubriken från "En fråga" till "Titrering av svag syra med stark bas". Det står i Pluggakutens regler att rubriken skall tala om vad frågan handlar om, och en fråga som heter "En fråga" kan handla om bokstavligt talat vad som helst. /moderator


Där är självaste frågan
Det står precis steg för steg vad du skall göra.
Visa hur långt du har kommit och var du kör fast, om du gör det.
När ska man använda ICE och när är reaktionen reversibel?
När det är en jämvikt, d v s när antingen syran eller basen är svag. Ättiksyra är en svag syra.
Jag har kommit till steg B men kan inte fortsätta därifrån
Det vill säga jag kan inte lösa c och d
Visa vad du har kommit fram till på fråga a och b - de delresultaten behövs för att du skall kunna gå vidare.
Tänk dig att reaktionen är kvantitativ, d v s att alla hydroxidjoner reagerar med äkktisyramolekylerna. Hur många mol acetatjon och hur många mol ättiksyra skulle det finnas i så fall? Detta är utgångspunkten för jämvktsberäkningen, "efter reaktionen men före jämvikt".
Det skulle finnas samma, men jag vet inte hur jag ska tillväga gå på beräkningen..
Först skrev jag x^2\x-0,04= Kb för syran, men det gick ej och fick fel svar.
Varför får jag ingen hjälp?
Du skall inte börja med jämviktsberäkningarna riktigt än. Först behöver du ta fram koncentrationerna "efter reaktionen men före jämvikt".
Hur gör man det? Jag har inte lyckats med den biten
Det var min första fråga jag ställde igår. Kan ni inte besvara hur man gör??
0,03 mol hydroxidjoner reagerar med 0,03 mol ättiksyra så att det bildas 0,03 mol acetatjoner. Hur många mol ättiksyra finns kvar? Detta är startpunkten för själva jämviktsberäkningen.