Energinivån-
 hejsan
hejsan
skulle jag få lite tips att komma igång med uppgiften?
ska man använda sambandet v=lambda •f?
eller omvandla till joule?
Det finns ett samband för energin hos en foton som säger att
Ta reda på vilken energi våglängden motsvarar (och omvandla gärna till eV).
Se sedan om du kan hitta en energidifferens i diagrammet som motsvarar den framräknade energin.
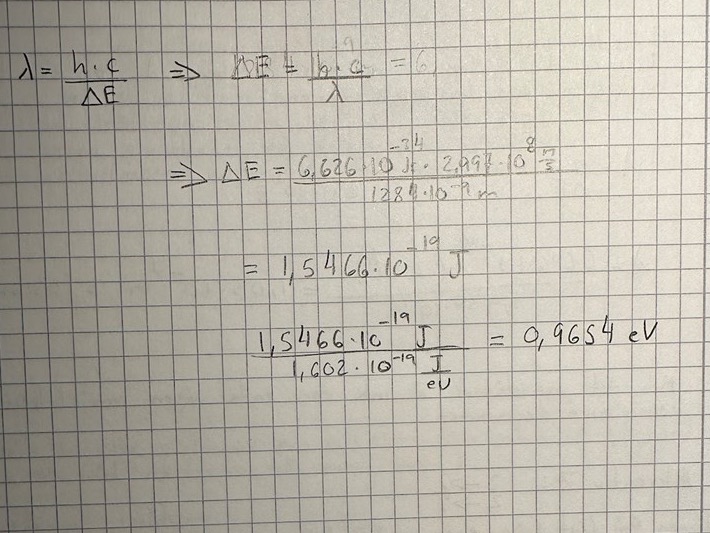 vad är nästa steg?
vad är nästa steg?
ska man testa sig fram Eföre-Eefter?
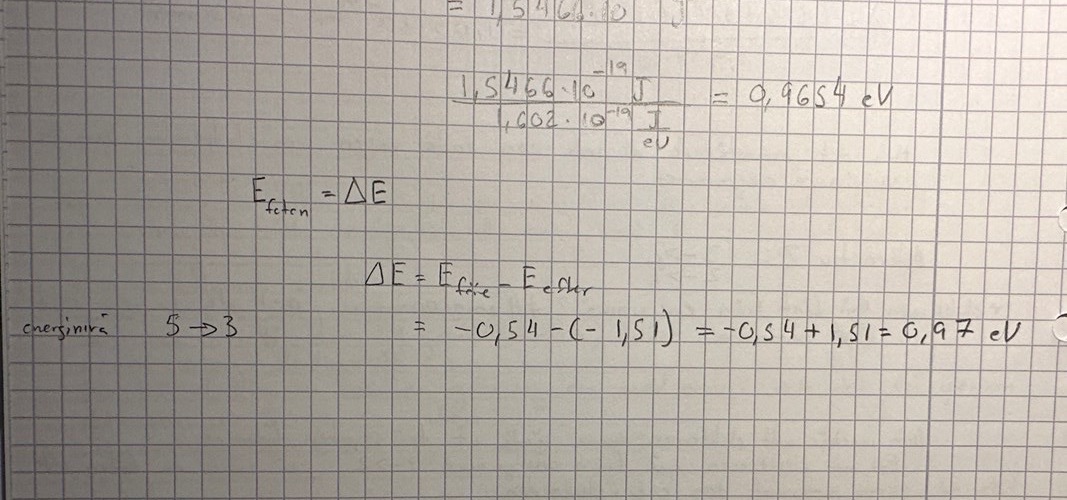 måste man testa sig fram hela tiden? Nu började jag av en slump uppifrån nedåt. Åt vilket håll ska man börja ifrån ?
måste man testa sig fram hela tiden? Nu började jag av en slump uppifrån nedåt. Åt vilket håll ska man börja ifrån ?
Likaså kan elektronen också ha direkt gått ner vilken nivå som helst
Japp, det ser bra ut. Övergången ligger i Paschen-serien och kallas eller Paschen-beta. Elektronen avger en foton motsvarande energiskillnaden mellan nivå 5 och 3.
Mycket bra detektivarbete!
Och den kan inte riktigt ha gått ned från vilken nivå som helst, notera att nivåerna ligger tätare och tätare ju längre upp du går, samt att det bara finns en tillåten övergång med ett delta på ungefär 1eV.
Energinivåerna i väte ges av
Och om du tänker efter är "skillnaden" mellan två nivåer mindre och mindre i takt med att växer kvadratiskt.
Det var något samband som jag inte minns ordentligt med att fotonens våglängder blir kortare (eller större) ju närmare elektronen kommer till grundstillståndet ?

