Entropiändring för Naftalen
Jag skulle behöva hjälp med denna uppgift.
¨Beräkna förändring av entropin för 10 g naftalen, C10H8(s), som först uppvärms från
rumstemperatur (298 K) till smältpunkten (vid 1 bar tryck), smälter och sedan vätskan uppvärms
vidare till kokpunkten och förångas fullständigt vid denna temperatur, e. g. vid kokpunkten och 1
bar tryck. (OBS: värmekapacitet för C10H8(s) och C10H8(l) är ej konstant utan är funktion av
temperatur!)¨
Ekvationen som ska användas är denna.

Men jag har problem med värdena för C(s), C(l) och C(g). Lika förstår jag inte helt hur man ska beräkna DHfus/DHvap.
Det fattas info för att man skall kunna lösa uppgiften. Det står i uppgiften att Cs och Cl inte är konstanta, utan varierar med temperaturen - ni måste ha fått någon info om hur de ändras för att man skall kunna lösa uppgiften. Och i den sista integralen skall väl båda gränserna vara Tvap?
Det där är all info som ges! Det med gränserna i sista är jag osäker över.
Enligt uppgiften skall sluttillståndet vara att temperaturen är vid kokpunkten och allt har förångats.
Du skall nog leta i din lärobok efter hur värmekapaciviteten förändras med temperaturen.
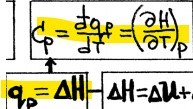
Hittade dessa ekvationer, men får ändå inte till rätt svar.
Sen är värdena för Tfus= 353,4 K , Tvap= 491 K , DHfus= 18,80 kJ/mol , DHvap= 51,51 kJ/mol .
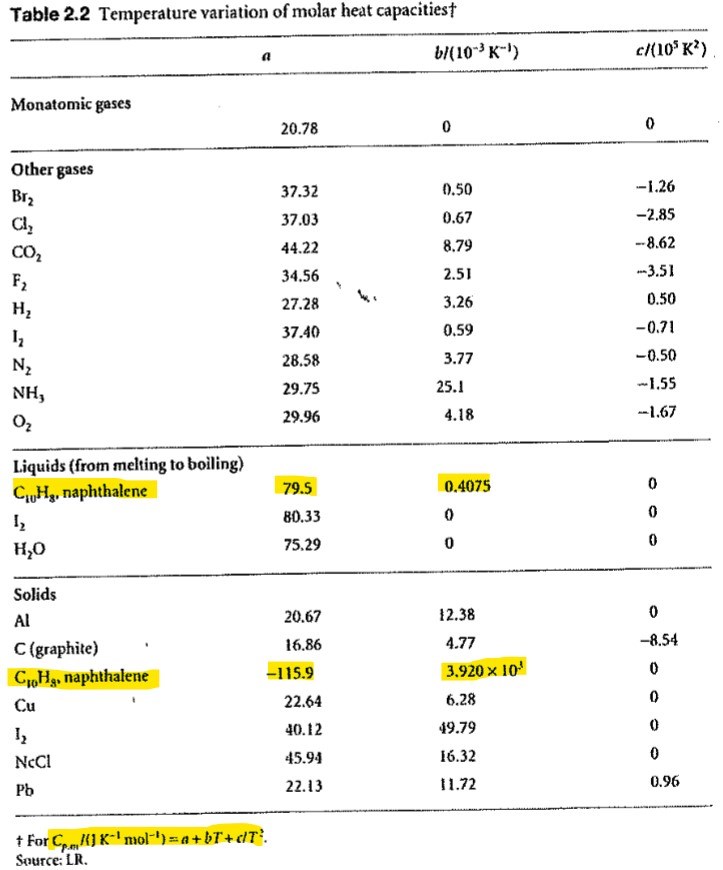
Här är hur man ska beräkna C(s) och C(l). Men jag får inte till rätt svar. Enligt facit är rätt svar 29,93 J/K
Visa steg för steg hur du gör dina beräkningar, så har vi en chans att hjälpa dig att hitta var det blir konstigt.


