Enzymet katalas i en sur/basisk miljö?
Hej! Jag har labbat med enzymet katalas och undersökt hur olika faktorer påverkar enzymets funktion. Min fråga är nu varför katalas slutade "funka" när man hällde ner saltsyra. Vi hade ju väteperoxid + lever + saltsyra kontra väteperoxid + lever + natriumhydroxid. Enzymet hos syran slutade då "funka". Varför det?
Min gissning är att de extra protonerna från syran började binda sig med katalaset, vilket denatuerade proteinet/förstörde den. Varför funkar det nu inte samma sak med basen? För när vi hade katalset i basisk miljö så "funkade" den nästan som vanligt.
Vilken var volymen HCL som tillsattes, och vilken var koncentrationen? Vet du till och med vilket pH det blev?
Vilken var volymen NaOH som tillsattes, och vilken var koncentrationen? Vet du till och med vilket pH det blev?
Att pH påverkar proteiner som enzymet katalas är ett generellt fenomen. Samtidigt är enskilda enzymer anpassade för att arbeta i ett individuellt pH-spann. T.ex. pepsin som är aktivt i magsäcken jobbar på väldigt effektivt i magsäckens mycket låga pH, bäst vid pH 1,5-2. Nästan alla andra proteiner denaturerar vid ett så extremt lågt pH, vilket naturen har utnyttjat - för när de andra proteinerna denaturerat kan pepsinet enklare klyva proteinerna i mindre bitar.
När magsäcken sedan tömmer sitt (av syran och pepsin delvis upplösta) innehåll ut i tolvfingertarmen följer så klart pepsinet med. I tolvfingertarmen möts pepsinet av det basiska bukspottet och pH stiger då upp till 8 - vilket får pepsinet att denaturera. Men samtidigt kommer andra enzymer som utsöndras i bukspottet vara mest aktiva vid pH 8 och fortsätta bryta ned tarmens innehåll (och även pepsinet, men det har gjort sitt).
Så att vilket pH intervall ett enzym är aktivt inom beror på var det naturligt återfinns, och den kemiska miljön (med bl.a. pH).
Vet du vilket pH intervall som katalaset är som mest aktivt inom? Det skulle nog göra det lättare att besvara din fråga...
Vid pH 7. Jag tror dock att saltsyran var lika stark som natriumhydroxiden. Det var en väldigt stor felkälla isåfall, även om man tar hänsyn till att jag kanske hällde lite mer saltsyra än natriumhydroxid i de motsvarande provrören, för vid basen så funkade reaktionen ganska bra, medan syran knappt funkade alls.
Saltsyra är en stark syra, och hydroxidjonen är en stark bas. Om de är "lika starka" eller inte beror på om deras koncentration är lika.
Din observation, att katalasaktiviteten, försvann efter tillsatsen av syran verkar rimligt.
Det är svårt att exakt veta pH i levermaterialet, men du kan nog anta att pH är nära blodets pH 7.4 (pH bör vara nära detta även inuti cellerna). pH optimum för katalas är nära 8, men aktiviteten finns inom ett intervall av pH, precis som för andra enzymer. Figuren nedan kommer ifrån en studie där enzymaktiviteten (på y-axeln) för katalas från däggdjur jämförts vid olika pH. Din mosade levers ungefärliga pH är vid den gröna linjen - alltså nära den högsta aktiviteten.
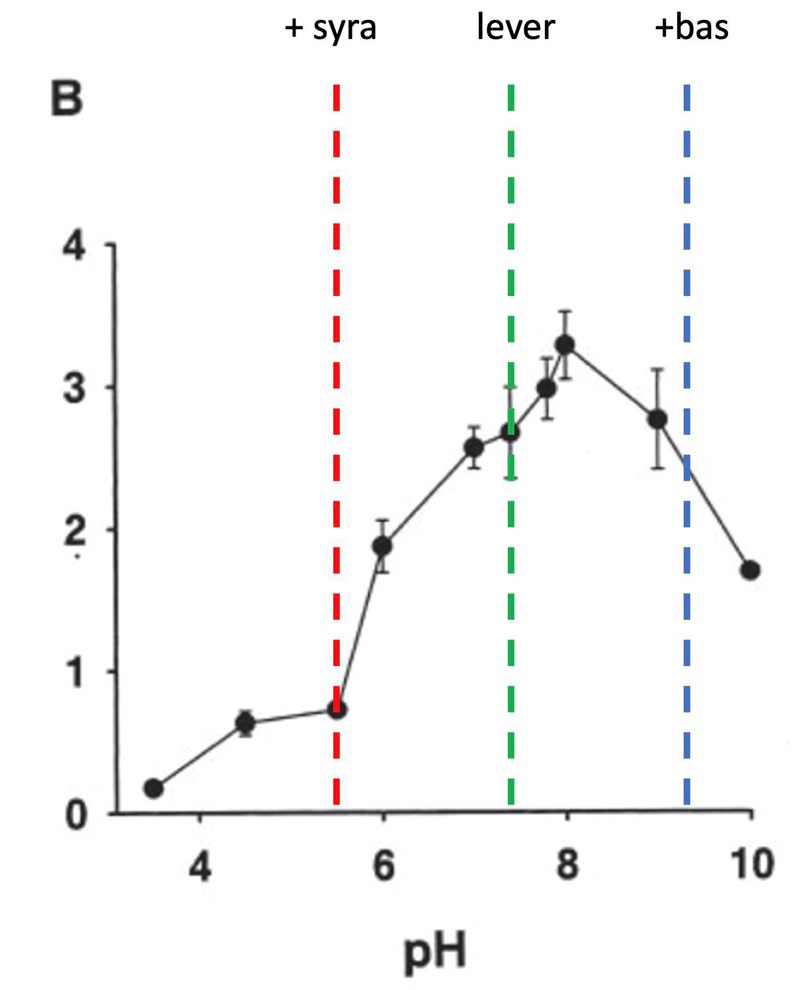
Om du tänker dig att pH förändras lika mycket uppåt som nedåt av basen/syran, kanske 2 enheter, så hamnar ditt katalas en bit från det optimala pH i båda fallen - men aktiviteten minskar olika mycket. Vid det lägre pH (röda linjen) har aktiviteten minskat med ca 75%, men vid det högre pH är minskningen betydligt mindre ca 15%.
Om ändringen av pH var ännu större, blir skillnaden i aktivitet ännu större (tills pH blir för högt och katalaset denaturerar av detta istället).



