fällning
En vattenlösning innehåller 100 g aluminiumsulfat. En annan vattenlösning innehåller 100g bariumklorid. När du häller samman de båda lösningarna bildas en fällning. Hur mycket väger den?
Al2(SO4)3
m = 100g
M = (27*2)+3(32+(4*16))=342g/mol
n = 100/342 =0,2924 mol
BaCl2
m = 100g
M = 137+35,5*2= 208 g/mol
n = 100/208 =0.4808 mol
jag vet inte ens vilken fällning det är som bildas antigen så är det AlCl3 eller BaSO4
Al2(SO4)3 + BaCl2 -->
hur går jag vidare nu?
Ett av de båda salterna är väldigt känt för att vara extremt svårlösligt, så svårlösligt att man kan dricka en uppslamning av det saltet om man skall röntga magtarmkanalen, trots att de lösliga salterna av denna metall är dödligt giftiga.
så vilket bildas?
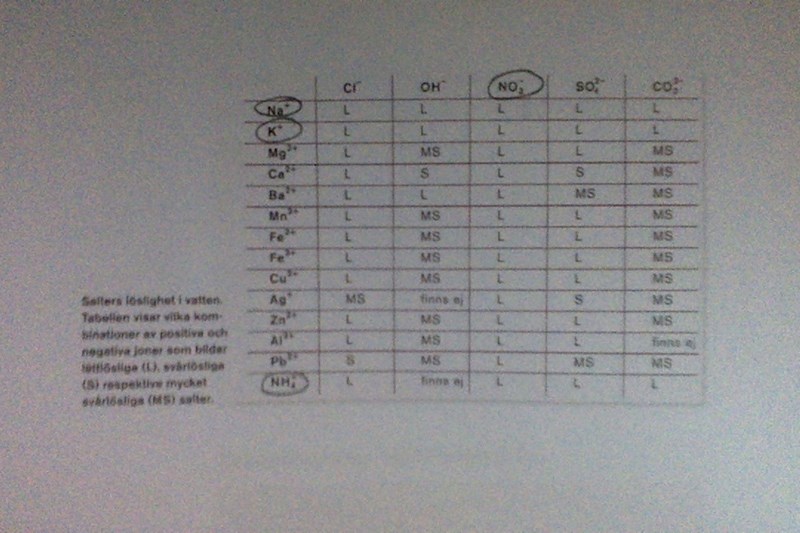
Men båda salterna är lättlösliga enlig den tabellen jag har som är väldigt trovärdig!
Då måste du har läst fel i tabellen. Vad står det? Lägg helst in en bild.
L är lättlösligt
S är svårlösligt
MS mycket svårlösligt
jag har löst den!!!
TAckkckck