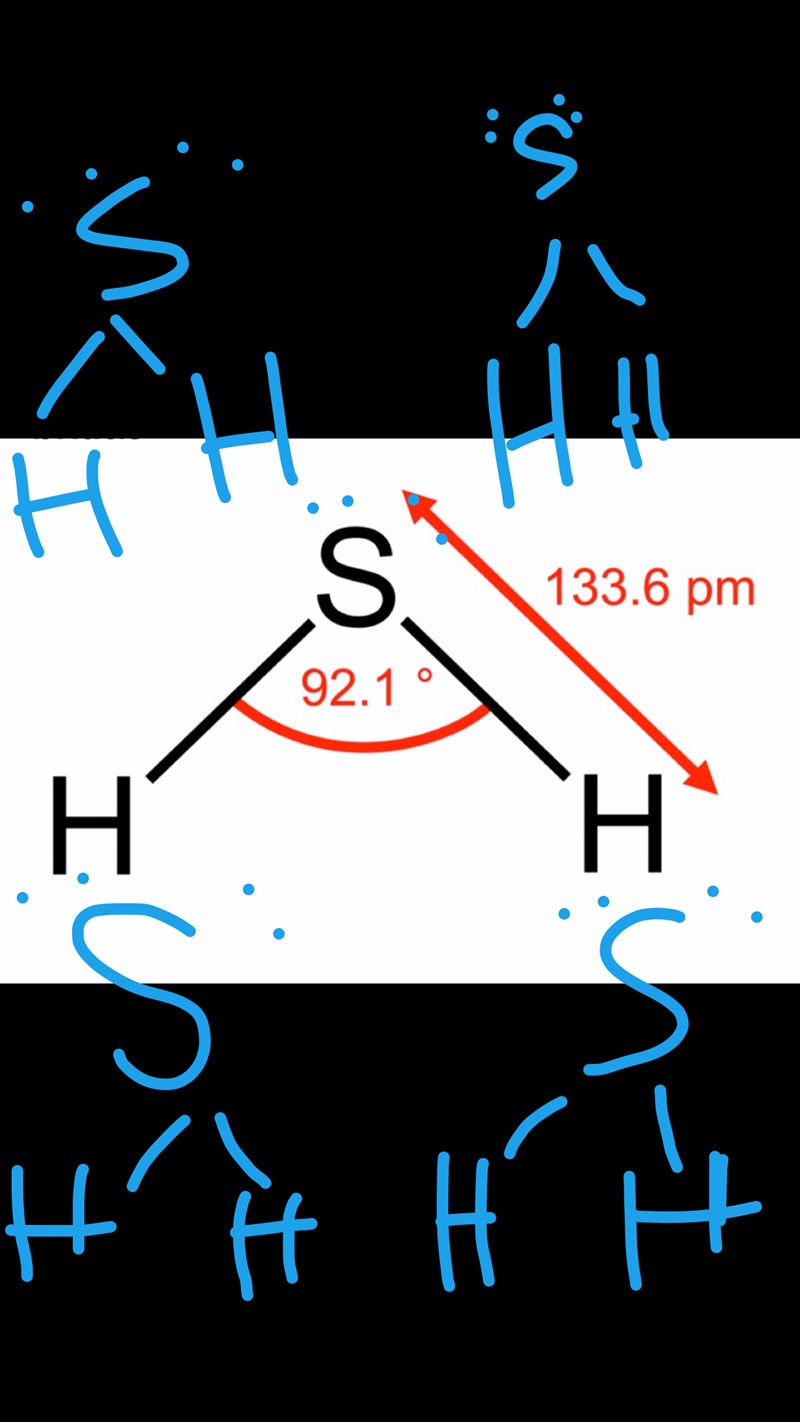
Hur många dipol dipol bindningar kan bildas
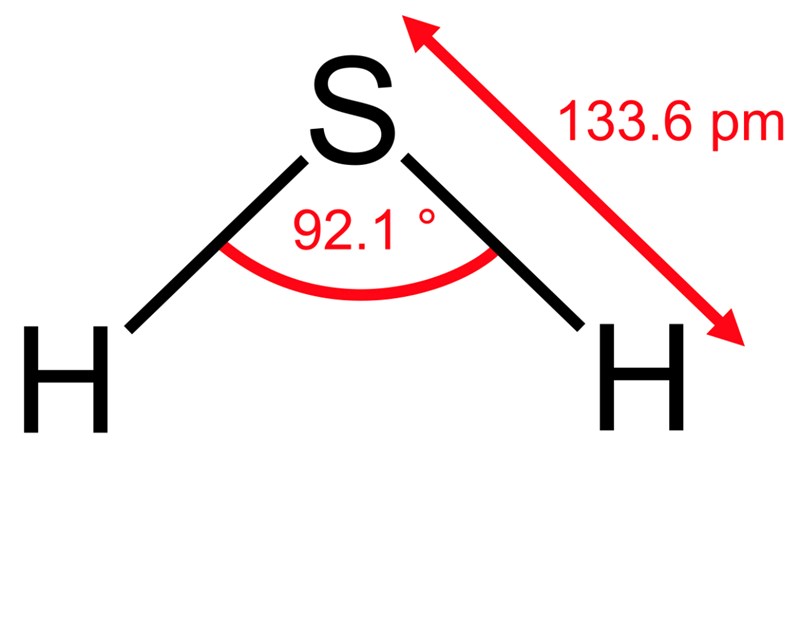 Hur många dipol - dipol bindningar kan svavelmolelylerna ingå i om det är svavelväte molekylerna som binder till varandra?
Hur många dipol - dipol bindningar kan svavelmolelylerna ingå i om det är svavelväte molekylerna som binder till varandra?
Mitt svar : Jag är osäker på hur jag ska tänka. Svavlet har 2 fria elektronpar. Dit skulle 2 svavelväte molekyler kunna binda. Alltså 2 svavelväte molekyler på atomen svavel. 1 elektronpar till varje svavelmolekyl. Därför kan man 2 svavelmolekyler bind till atomen svavel.
Väten som finns med har redan uppnåt ädelgasstrukturen och kommer inte uppta/ ingå i en dipol dipol binding Alltså 2 st dipol - dipol bindningar bildas genom svavlets 2 fria elektronpar.
Hur ska man tänka/rita? Tänker jag fel?
Svavelväte har samma elektronkonfiguration som vatten. Svavelväte kan bilda lika måga dipol-dipolbindningar som vattenkan bilda vätebindningar, d v s två som donator och två som acceptor, alltså 4 bindningar totalt.
Vilka atomer (svavel/ väte) är donator och vilka är acceptor?
Kan man illustrera det på följande sätt? :
Gula färgen visar att det finns en bindning mellan vätet och svavlet tackvare de fria elektronerna 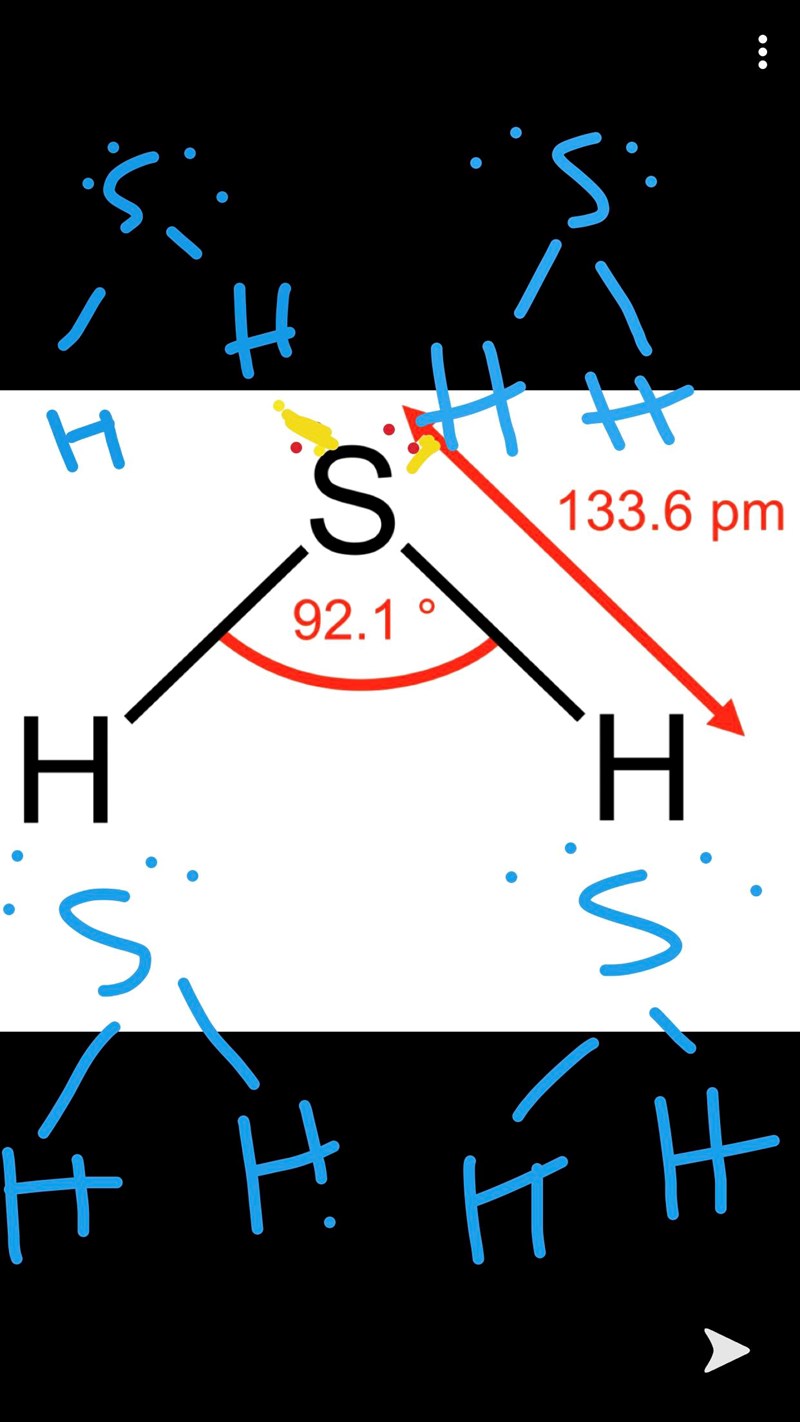
De övre gula markeringarna ser bra ut. Väteatomerna i nederkanten borde binda till ett av elektronparen på "nästa" vätesulfidmolekyl, inte båda.
Kanske bättre nu?