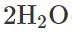hur resonerar de? +I oxred
Frågan:
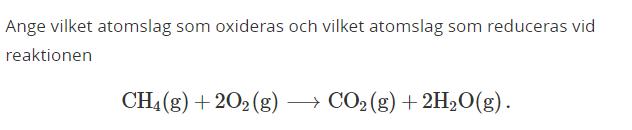
Jag:
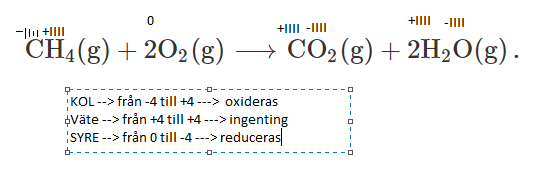
Facit:

Vi har samma slutsatser, men de får antalet till annat. Hur räknar de?
Vätet är jag inte riktigt med på hur de fick det till +I , det är väl 4 väte dvs +IIII (till en början)
och sedan efteråt är det (2 * 2 * I ) = +IIII där med?
Syre till en början = 0 (är jag med på) men att det sedan bli -II ? det är ju 2H2O , dvs ( 2 * - II ) = - IIII
Tror jag kommit på det, det är alltså laddningen för EN man skriver, och inte totala?
naturnatur1 skrev:Tror jag kommit på det, det är alltså laddningen för EN man skriver, och inte totala?
Just det, man räknar ut oxidationstalet för var och en av atomerna.
Smaragdalena skrev:naturnatur1 skrev:Tror jag kommit på det, det är alltså laddningen för EN man skriver, och inte totala?
Just det, man räknar ut oxidationstalet för var och en av atomerna.
Jaha, så man bortser alltså från siffror framför ämnena och de nersänkta talen? Exempelvis
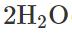
Så tar man bara hänsyn till att en väte har ox tal +I och syret -II ? (trots det finns 2 vattenmolekyler och 2 väteatomer)
Det är alltså inte som när man räknar med mol? (Hänsyn till nersänkta tal)
naturnatur1 skrev:Smaragdalena skrev:naturnatur1 skrev:Tror jag kommit på det, det är alltså laddningen för EN man skriver, och inte totala?
Just det, man räknar ut oxidationstalet för var och en av atomerna.
Jaha, så man bortser alltså från siffror framför ämnena och de nersänkta talen? Exempelvis
Så tar man bara hänsyn till att en väte har ox tal +I och syret -II ? (trots det finns 2 vattenmolekyler och 2 väteatomer)
Det är alltså inte som när man räknar med mol? (Hänsyn till nersänkta tal)
eller?
När man beräknar oxidationstal så tittar man på varje molekyl eller jon för sig, och varje atom i jonen eller molekylen för sig.
Smaragdalena skrev:När man beräknar oxidationstal så tittar man på varje molekyl eller jon för sig, och varje atom i jonen eller molekylen för sig.
ja men jag trodde exempelvis vätet hade oxidationstalet +4 (i början) då det fanns 4 väte.
men enligt facit hade den laddningen +1 ? (man tar inte hänsyn till helheten alltså?)
Nej, man räknar oxidationstalet för VARJE ATOM FÖR SIG. Fyra väteatomer med oxidatonstal 1 ger summan 4.
Smaragdalena skrev:Nej, man räknar oxidationstalet för VARJE ATOM FÖR SIG. Fyra väteatomer med oxidatonstal 1 ger summan 4.
Okej, det strular i huvudet för mig. Eftersom det var så jag tänkte initialt, att 4 väteatomer har OT 4 eftersom varje väte har OT 1, trots att det är 4 väteatomer?
Skulle du kunna förklara utifrån det exemplet jag har? Tack på förhand.
Fyra väteatomer med ox.tal +1 ger sammanlagt +4. För att summan skall bli 0 måste kolatomen ha ox.tal -4.
Man kan säga att summan av väteatomernas ox.tal är +4, men man kan inte säga att väteatomerna har oxidationstalet +4.