Identifiera ämnen
Hej.
Jag har fått i uppgift att identifiera 7 olika ämnen med valfria metoder.
Ämnena är heptan, citronsyra, glycerol, natriumsulfat, stearinsyra, natriumvätekarbonat och glycin
Har börjat med att göra en tabell över hur strukturen för ämnena ser ut.
Jag tänker att man enkelt kan identifiera stearinsyra för att den är i puder form. Sedan kan man testa ämnenas löslighet i vatten för att identifiera heptan som är det enda ämnet som inte är lösligt i vatten. Men hur kommer jag vidare från detta? Tänker jag rätt?

Du kan inte identifiera stearinsyra utifrån att det är ett puder. Dels för att det inte behöver vara i puderform, dels eftersom både citronsyra, natriumsulfat, glycin och natriumvätekarbonat också kan vara i puderform.
Heptan är inte lösligt i vatten, men det är inte heller stearinsyra. Hur vet du vad som är vad mellan dem?
Tips till övriga: Hur kan du identifiera syror och baser? Salter?
Jaha.
Syror och baser identifieras lätt med PH och salter med fällning.
Men det jobbiga för mig är att jag inte vet vad jag ska börja identifiera. Hittar ingen startpunkt.
Varför är stearinsyra inte lösligt i vatten? Om man utgår från strukturen så har den vätebindningar och är polär, vilket vatten också är. Därför tänker jag att lika borde lösa lika.
Stearinsyra har en lång kolkedja som gör föreningen opolär. Det är inte så enkelt som att en förening blir polär och därmed vattenlöslig för att det finns en liten polär grupp. Man måste ta hänsyn till hur hela molekylen ser ut.
Ett tips är att göra en tabell med en rad för varje ämne och egenskaper i kolumnerna. Sen kan du sätta ett kryss i rutorna för varje ämne som uppfyller egenskaperna. Om du har egenskapen ”Ger basiskt pH” skulle det bli ett kryss för natriumvätekarbonat.
okej men glycin är ju en aminosyra och aminosyror är ju amfolyter. Betyder detta att glycin löst i vatten kommer att ha ph 7?
Sedan när jag ska identifiera natriumvätekarbonat och natriumsulfat så tillsätter jag saltsyra till båda tuberna. Kommer natriumvätekarbonat att reagera med saltsyra och bilda en vit fällning? Och kommer natriumsulfat inte bilda en fällning? Kan man på så sätt skilja på dessa två ämnen?
okej men glycin är ju en aminosyra och aminosyror är ju amfolyter. Betyder detta att glycin löst i vatten kommer att ha ph 7?
Nej du kan inte dra den slutsatsen. Jag skulle säga att glycin är det svåraste ämnet av dessa att identifiera, så min strategi hade varit att identifiera övriga ämnen och sedan identifiera glycin med uteslutningsmetoden.
Sedan när jag ska identifiera natriumvätekarbonat och natriumsulfat så tillsätter jag saltsyra till båda tuberna. Kommer natriumvätekarbonat att reagera med saltsyra och bilda en vit fällning? Och kommer natriumsulfat inte bilda en fällning? Kan man på så sätt skilja på dessa två ämnen?
Du kan identifiera natriumvätekarbonat, liksom alla andra karbonater och väterkarbonater, genom att tillsätta saltsyra. Men du får inte någon fällning utan det börjar fräsa av koldioxid från blandningen. Syran reagerar med vätekarbonaten som bildar kolsyra, vilken direkt sönderfaller till koldioxid och vatten. Det brukar kallas för frästestet.
Om du blandar saltsyra och natriumsulfat händer ingenting.
Såhär har jag tänkt:
Först kan man identifiera heptan och glycerol genom att observera ämnenas utseende. Heptan och glycerol är de enda två ämnena som kommer att vara flytande vid rumstemperatur medan de andra fem ämnena förekommer i pulverform. Sedan kan man identifiera vilket eppendorfrör som innehåller heptan respektive glycerol genom att testa deras löslighet i vatten. Av de två är det endast glycerol som kan blandas med vatten. Glycerol är fullständigt lösligt i vatten på grund av dess höga polaritet och förmåga att bilda vätebindningar. Heptan å andra sidan är fullständigt opolärt och kan därför inte alls blandas med vatten. Heptan kommer att lägga sig som ett skikt ovanpå vattnet eftersom den har lägre densitet.
Efter att heptan och glycerol identifierats kommer stearinsyra att identifieras. Bland de fasta ämnena har stearinsyra den lägsta smältpunkten: 69,3 °C. Substansen med den näst lägsta smältpunkten är citronsyra: 153 °C. Att smältpunkten för glycerol och stearinsyra skiljer sig med 83,7 °C gör det enkelt att identifiera stearinsyra. Man värmer upp de fasta ämnena i ett vattenbad vid cirka 80 °C för att observera vilka ämnen som smälter. Det ämnet som smälter är stearinsyra.
Sedan kör jag fast. Jag har Natriumvätekarbonat, natriumsulfat, citronsyra och glycin kvar att identifiera. Vad ska jag identifiera härnäst?
Ser bra ut hittills! Natriumvätekarbonat har du redan hittat ett sätt att identifiera, genom att tillsätta saltsyra. Övriga tre ämnen skulle jag nog identifiera utifrån deras syrabasegenskaper. En lösning av natriumsulfat är neutral, så den kan man lätt särskilja.
Citronsyra och glycin är svårare eftersom vattenlösningar av dessa två är sura. Det man kanske kan utnyttja är att glycin även kan fungera som bas vilket inte citronsyra kan göra. Tillsätter man lite av en stark syra borde pH sjunka mindre i den lösning som innehåller glycin.
Tack för dina snabba svar förresten!
pH i bägge lösningarna sjunker om du tillsätter en syra. Det är lågt från början eftersom citronsyra och glycin i sig är syror, men det blir ännu lägre om du tillsättet t.ex. saltsyra. Däremot kan en del glycin reagera med saltsyran och ta upp vätejoner - det är ju en amfolyt som även kan fungera som bas vid tillräckligt lågt pH. Detta kan inte citronsyra göra. Alltså sjunker pH mer i den lösning som innehåller citronsyran.
okej men natriumsulfat är svagt basisk och saltsyra är en stark syra. Då kommer väl inte blandningen bli neutral utan mer sur? Måste jag då blanda en liten mängd saltsyra till substanserna. Kommer jag då kunna se att natriumvätekarbonat fräter?
Lösningen med natriumsulfat är den enda som inte blir sur, så du kan identifiera den utifrån det. Du behöver inte tillsätta någon saltsyra i det provet.
okej så jag behöver först tillsätta lite vatten i alla provrör med de 4 okända substanserna som har en puder form och sedan mäta deras pH. Jag kan då konstatera att det ämnet med högst pH kommer att vara natriumsulfat. Sedan tillsätter jag saltsyra till de 3 kvarstående provrören med de okända substanserna och drar slutsatsen om att ämnet som fräter är natriumvätekarbonat. Sedan mäter jag pH på de två sista okända substanserna och kontaterar att det ämnet med lägst pH är citronsyra och det med ett högre pH än saltsyra är glycin.
Är detta rätt nu?
fast det går inte att göra så för att natriumsulfat och natriumvätekarbonat är båda svaga baser och har ett pH>7 då kan jag ju inte konstatera vilket av substanserna som är natriumsulfat. Hur ska jag göra då?
Natriumsulfat är i praktiken neutralt även om det i teorin kan anses vara väldigt svagt basiskt. Men det spelar ingen roll, för natriumsulfat fräser inte om det kommer i kontakt med saltsyra vilket däremot natriumvätekarbonaten gör. Det är så du ser skillnad mellan dem.
Sara.s0, det är aboslut inte tillåtet att redigera bort ett inlägg efter att din tråd har besvarats. Nu är tråden omöjlig att följa, och Teraeagles svar på dina frågor är helt obegripliga. Trådarna här på Pluggakuten är tänkt att fungera som en kunskapsbank. Läs igenom reglerna om du inte vet vad som gäller. Frekventa regelbrott kommer leda till en avstängning. /Moderator
Jaha oj. Jag visste inte det. Ber om ursäkt.
Jag ska identifiera ämnena natriumsulfat, citronsyra, glycin och natriumvätekarbonat. Jag har löst upp ämnena i vatten och tillsatt BTB för att se vad deras ph är. Detta blev resultatet:

Vad kan jag identifiera utav detta?
Vad tyder det på när BTB får dessa färger?
Citronsyra är den gula och natriumvätekarbonat är den blåa. Så vi kan identifiera dessa. Vi har dock två ämnen kvar. Glycin och natriumvätekarbonat. Vad är det man kan testa för att identifiera dessa?
Glycin och natriumsulfat är de som återstår, menar du kanske?
Man kan ana är kolven näst längst till vänster är lite mer gröngul vilket betyder att den är mer åt det sura hållet än kolven näst längst till höger som också har en grönaktig färg. Glycin kan verka som syra, vilket inte natriumsulfat kan göra. Så glycin bör finnas i kolven näst längst till vänster.
Detta är inte glasklart, men om du inte ska/kan göra fler tester är det den slutsats man får dra.
Jag kan göra fler tester. Men varför kan glycin verka som en syra men inte natriumsulfat?
Kan natriumsulfat avge vätejoner?
Jaha nu fattar jag. Men vad kan man uttligare testa för att skilja på glycin och natriumsulfat. Kanske fällning?
Kan funka, om man hittar något reagens som bara ger fällning med det ena ämnet. Vilket ämne skulle du i första hand försöka fälla ut? Det finns ett välkänt reagens som kan användas på något som finns i den ena kolven.
Bariumhydroxid och natriumsulfat bildar fällning.
Ja det stämmer. Tillsätter du bariumjoner får du fällning i det rör som innehåller sulfatjoner.
Problemet är att vi inte vet om bariumjonerna även kan reagera med (den korresponderande basen till) glycin. Man skulle kunna fälla ut bariumglycinat, men det är ett så ovanligt ämne att det är svårt att hitta uppgifter om det.
Jaha. Finns det ett annat ämne som är bättre att använde när man vill testa fällning på de två ämnena.
Nja, jag hade testat bariumjoner. Om du får fällning i bara det ena fallet vet du att det är den med natriumsulfat.
Hur ska jag förklara att glycerol och heptan är flytande i rumstemperatur medans natriumvätekarbonat, glycin, citronsyra, natriumsulfat och stearinsyra är i fast form?
Jag tänker att heptan är enkel att förklara för att den endast har VDW bindningar vilket är svaga bindningar men glycerol är polär och har vätebindningar. Varför är den i flytande form vid rumstemperatur?
Kanske lite svårt att förklara kemikaliernas aggregationstillstånden i rumstemperatur så ska hoppa över det. Men det jag inte heller förstår är varför natriumsulfat har ett neutralt pH. Har någon en bra förklaring till det?
Den korresponderande syran till sulfatjonen, dvs vätesulfatjonen, är tillräckligt stark för att sulfatjonen ska bli en obetydlig bas. Det är så det fungerar - desto starkare korresponderande syra, desto svagare korresponderande bas. Natriumjonerna saknar helt syrabasegenskaper.
Jag tror inte jag riktigt förstår. Har glömt vad korresponderande syra betyder hade det i kemi 1. Skulle du kunna förklara det begreppet?
Det du får om en vätejon binder till ämnet.
Okej men finns det en bra förklaring till varför glycin är mer sur än natriumsulfat?
Glycin är ju en syra (aminosyra) som kan avge vätejoner, vilket inte natriumsulfat kan göra.
Har jag tänkt rätt här?
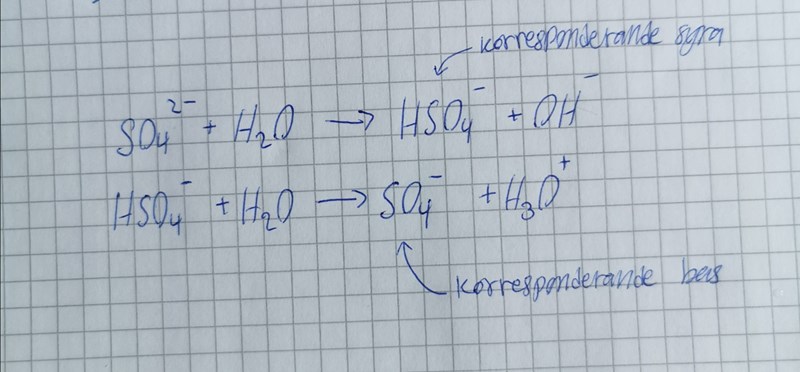
Har försökt skriva ut alla reaktionsformler för när ämnena blandas med vatten och förklara utifrån formlerna varför ämnena får det pH de får. Kör fast vid glycin. Kan man säga att glycin har en neutral sidokedja vilket gör att dess ip ligger på 6 och därmed också dess PH-värde. Att dens ph värde inte är neutralt beror ju på att karboxylgruppen är en starkare syra än aminogruppen som är en svagare bas.
Är reaktionsformlera korrekta?

Citronsyra är ju en syra så den kommer att få en gul färg. Natriumvätekarbonat är en bas och kommer därför få en blå färg. Men sedan fastnar jag på natriumsulfat och glycin. Natriumsulfat är ju ett neutralt salt för att sulfatjonens korresponderande syra, vätesulfatjonen, är så stark att den kan protolyseras. Detta gör ju att sulfatjonen blir en obetydlig bas. Därför får en lösning av natriumsulfat ph 7, grön färg. Glycin är ju en aminosyra med en neutral sidokedja, bara ett väte, detta gör ju att dens ip ligger på 6 och därmed också dess ph. Fastän glycin är en amfolyt så har den inte ett neutralt ph för att karboxylgruppen är en starkare syra än aminogruppen som är en svagare bas. Därför kommer glycin reagera mer som en syra än som en bas och få en mer ljus grön färg än natriumsulfat som har en mörkare grön färg. Tänker jag rätt?
Ja, ungefär så skulle jag också ha resonerat.