Ingen protonöverföring
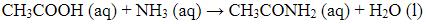
Förstår inte varför CH3COOH inte räknas som en bas i detta fall, och NH3 som en syra.
NH3 donerar ju en proton till CH3COOH (som accepterar den)
Facit säger "Ingen proton överföring", men varför är det så?
Svaret kanske ligger i hur en "proton överföring" betraktas. Blandas syran och basen, bildar de gärna ammoniumacetat i vatten, och saltet kan under upphettning ge acetamiden. Ättiksyrans hydroxigrupp lämnar ju som vatten, och den extra protonen tas nettomässigt från ammoniakmolekylen.
Men, ammoniumjonen saknar ju ett fritt elektronpar, och kan då inte bilda den nya bindningen till karbonylkolet, till skillnad från ammoniak. Så den reagerande formen är ammoniaken, trots det efter blandningen av syran och basen, finns endast en liten andel ammoniak i lösningen. Det är kanske det som åsyftas med "ingen proton överföring".
Klassiska syra-bas reaktion mellan ättiksyra och ammoniak är bildning av två joner i form av saltet ammoniumacetat.
I den reaktionen som du skriver bildas en ny neutral molekyl i form av amid i en kondensationsreaktion (inget salt som i en klassiskt syra bas reaktion där en proton överförs.)
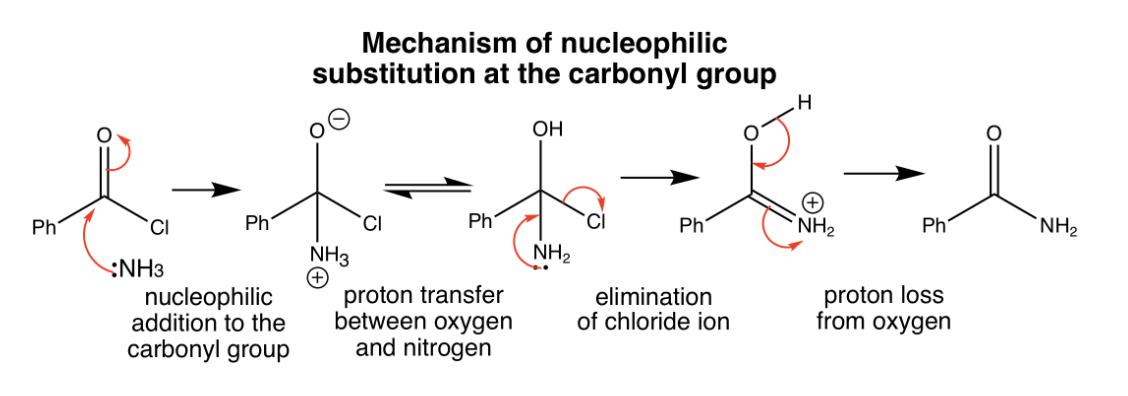
Om man tittar noggrann, så finns det faktist en intramolekular syra-bas reaktion där en proton transfereras, men det är bara en delsteg. I stort sätt är det här en nukleofil substitution.
Jag tror att meningen med frågan i facit är att framhäva skillnaden mellan en enkel proton transfer där en salt bildas och en komplexere kondensationsreaktion där neutrala reaktionsprodukter uppstå (och protontransfer är bara temporärt och intramolekular).
(Här ett exempel med -Cl istället för -OH i ättiksyra eftersom den är lättare att få bort)