Isoelektriska punkten
Hej!
Jag skulle behöva hjälp med en fråga angående isoelektriska punkten inom biokemi. Jag vet att om pKa är större än pH så kommer det vara ett överskott på protoner. Men jag har tre olika pKa världen och vet inte hur jag ska förhålla mig till det? Handlar det om jämviktsreaktioner eller vad ska man använda sig av? Och asparaginsyra har redan en negativ laddning från början, hur ser den då ut när den räknas som amfojon?
mvh,
Elsa
Tyvärr laddas inte bilden du lade upp, det enda jag ser är "Visar IMG-0026.jpg", men jag provar att svara ändå.
Elsaschuttler skrev:Hej!
Jag skulle behöva hjälp med en fråga angående isoelektriska punkten inom biokemi. Jag vet att om pKa är större än pH så kommer det vara ett överskott på protoner.
Nja, koncentrationen av hydroniumjoner (H3O+), det som ofta lite slarvigt kallas "protoner", är vad den är i lösningen.Aminosyrans protolys/upptag av protoner beror på den funktionella gruppens pKa.
Men jag har tre olika pKa världen och vet inte hur jag ska förhålla mig till det? Handlar det om jämviktsreaktioner eller vad ska man använda sig av? Och asparaginsyra har redan en negativ laddning från början, hur ser den då ut när den räknas som amfojon?
mvh,
Elsa
Ja varje protolysreaktion är en jämviktsreaktion, men jämvikten förskjuts beroende av pH.
Alla aminosyror har en karboxylsyragrupp och en aminogrupp, vilket ger två av pKa värdena. Och dessa grupper har vid neutralt pH varsin laddning p.g.a. protolys (COOH till COO-) samt upptagande av en proton (NH2 till NH3+), d.v.s. amfojonen.
De aminosyror med en laddad sidokedja har ytterligare ett pKa värde. Och vid neutralt pH kommer sidokedjan ge en nettoladdning (en negativ laddning från karboxylsyran, en positiv laddning från aminogruppen = noll. Plus positiv eller negativ laddning från sidokedjan). Men samtliga gruppers laddning påverkas av pH.
Så för ditt exempel med asparaginsyra, är dess tre pKa värden 2 (α-karboxylsyragruppen), 3,9 (sidokedjan), 9,9 (aminogruppen). Vid neutralt pH är samtliga grupper laddade, men kring pH 4 saknas laddning (då sidokedjan saknar laddning och de två andra gruppernas laddningar tar ut varandra). Så asparaginsyran kan laddningar från minus ett till plus ett, beroende på pH.
- Ok okey det var inte meningen med bilden. Här är den om det fungerar

- Uppgiften handlade om asparaginsyra. Men förstår fortfarande inte hur man ska koppla ihop flera olika pKa? Jag kan ju göra om dem till pH men då vet jag inte hur jag ska koppa tre olika pH vården. Hur ska jag veta att syra är oladdad vid pH4? Eller är det bara något att lära sig?
Det inte helt korrekt det jag skrev, med pH 4.
Vid ett ämnes pKa är hälften av molkeylerna i basformen och hälften i syraformen, så i ditt exempel med asparginsyran är 50% av molekylerna i basformen (de har protolyserats, COO-) och den andra hälften är i syraformen (har inte protolyserats, COOH) sidokedjans. Eller vid pH 3,9 är varje molekyl 50% chans att vara protolyserad.
Så om pH sänks med en enhet finns det väldigt få molekyler kvar i basformen, vilket du ser då dess isoelektriska punkt är 3. Det är då aminosyran saknar laddning.
Så för a) är pH väldigt nära Ip, och då finns det i särklass mest av den formen av asparginsyra med sidokedjan i syraformen.
Kommer du vidare med alfa-karboxylen/aminogrupperna?
Behöver jag räkna ut varje sidogrupps form (bas/syra/neutral) genom att jämföra pH förändringen för att få fram hela asparaginsyras hela form för varade uppgift? Eller var uppgift a klar där?
Du behöver lista ut vilken form (syra/bas) som dominerar för de respektive grupperna, och summera deras laddningar. För a) fick du i uppgiften reda på Ip, så då är svaret per definition att laddningen är noll (då alfa-karboxyl-/aminogruppernas laddningar tar ut varandra).
b) och c) behöver du titta på samtliga grupper.
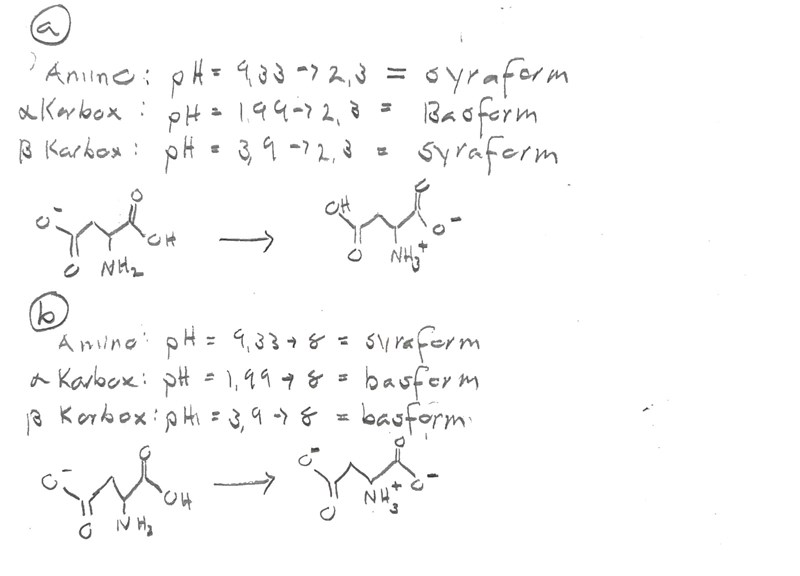
Har ställt upp det såhär och fick rätt svar men vet inte om det är korrekt skrivet. Är resonemanget rätt/ går det att följa?