Jämvikt, störst substansmängd?
Hej i min uppgift ur kemiboken står det såhär:
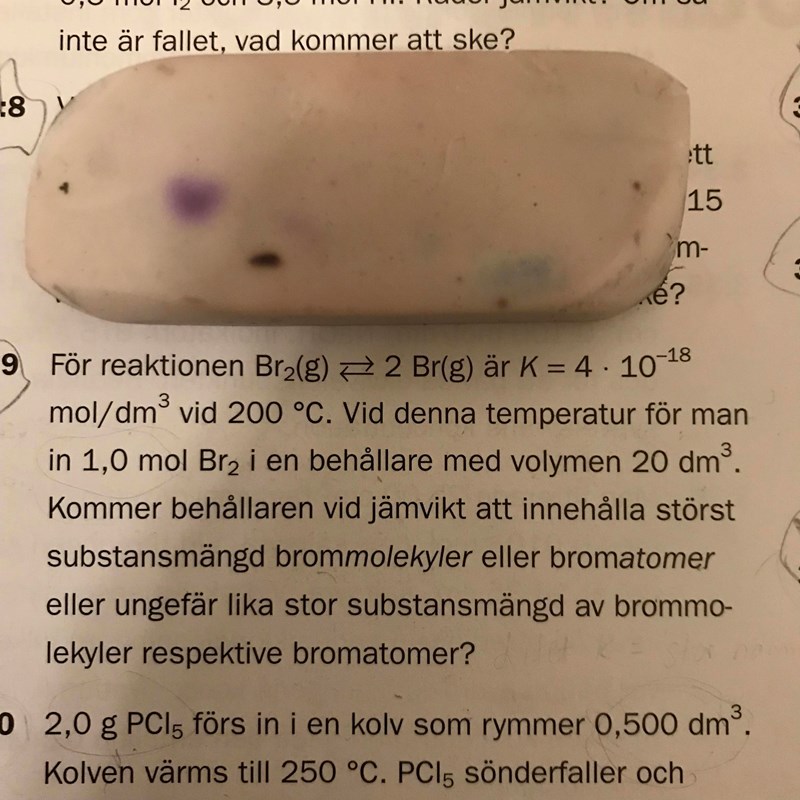
Och jag tänkte att man kunde kanske diskutera detta i termer om Q och K. Men jag fick fel och jag undrar om någon vet varför msn inte kan göra så?
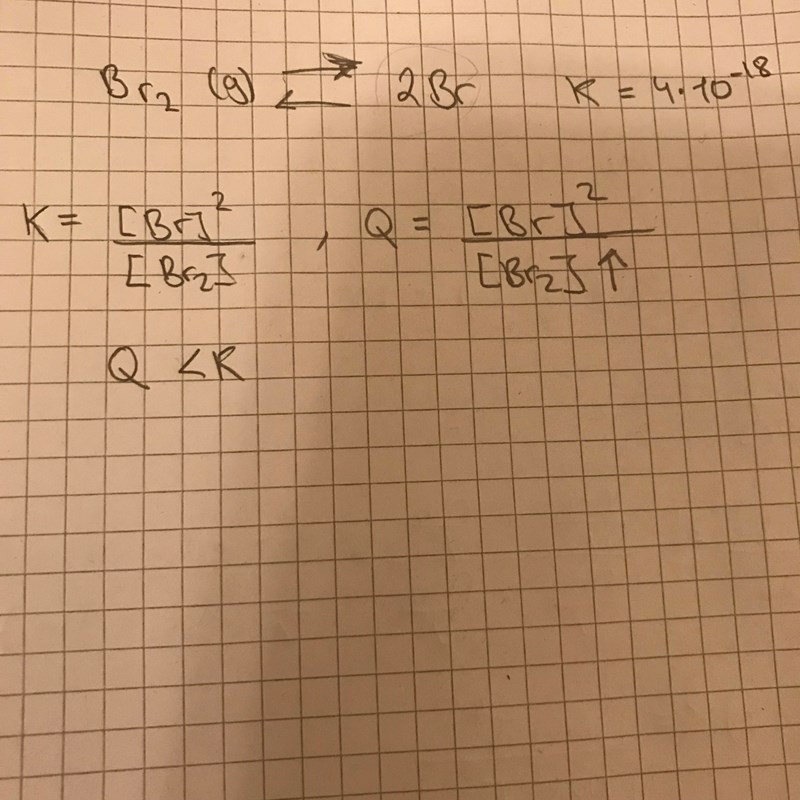
Det kommer att finnas betydligt mer Br2 än Br. Kvoten mellan koncentrationerna (där den ena koncentrationen visserligen är i kvadrat) är så liten som 4*10^(-18). Då har man betydligt mer Br2 än Br vid jämvikt.
Teraeagle skrev :Det kommer att finnas betydligt mer Br2 än Br. Kvoten mellan koncentrationerna (där den ena koncentrationen visserligen är i kvadrat) är så liten som 4*10^(-18). Då har man betydligt mer Br2 än Br vid jämvikt.
Ah så på grund av att jämviktskonstanten K är så liten så finns det mer utav Br2 än Br om man tänker matematiskt. Men det jag fortfarande inte fattar är varför man inte kan diskutera det med hjälp av K och Q. Då blir det fel?
Det hade varit intressant att om man frågade efter åt vilket håll reaktionen kommer att gå (nu har man ju 0 mol av produkten vid start, så den kan egentligen bara gå åt höger). Om man frågar efter hur mycket som finns vid jämvikt så är det alltid K som är av intresse.
aha okej tack så mycket!!! :DDD
Du vet ju inte koncentrationerna vid jämvikt (du skulle kunna räkna ut dem). När man släpper in brommolekyler i behållaren, är ju koncentrationen av bromatomer 0 och då kommer reaktionen att gå åt höger. Om x mol brommolekyler sönderfaller, så kommer det att bildas 2x mol bromatomer och finnas kvar 1-x mol brommolekyler. Om man sätter in detta i jämviktsekvationen kan man räkna ut koncentrationen av brpmatomer, om man skulle vilja.




