Kemi mysteri 2: tillfört energi för att smälta gaser vs alkalimetaller
När man kollar på ädelgas smältpunkt märker man att de kräver mer och mer energi för att smälta när vi går ner i den periodiska system. Som verkar logisk, det är ju större ädelskal att krossa som pilas upp på varandra!

Däremot det funkar tvärtom för alkalimetaller. Det krävs ju mindre och mindre energi för dom metaller med dom storsta skal? Betyder det att det räcker att ta bort den valens elektron för att få alkalimetallen att smälta? Men isf borde det inte vara en alkalijon? Kan inte förstå saken...
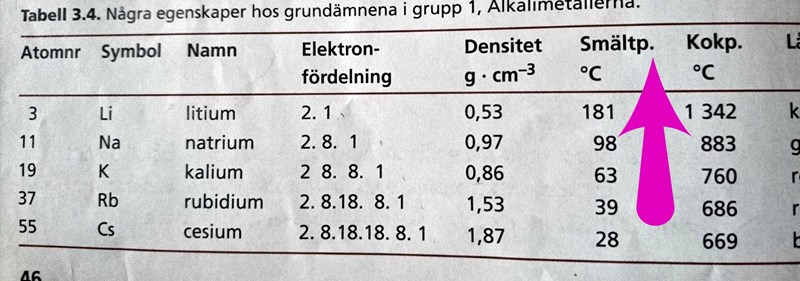
Det ser ut som om du har missat ett minustecken. I båda fallen gäller ju att de minsta atomerna hör ihop med de lägsta smältpunkterna och de minsta krafterna som behöver övervinnas.
Nej, man kan inte få ett ämne att smälta genom att ta bort en elektron från den. Ett ämne smälter när värmerörelserna blir stora nog att bryta sönder de sammanhållande krafterna (v d W för ädelgaserna, starkare metallbindning för alkalimetallerna).
Fast metallbindningen borde bli starkare när jonerna är mindre.
Avståndet från kärnan till ledningselektronerna är mindre för Li än för Cs, vilket gör att metallbindningen är starkare för Li än för Cs. Starkare metallbindning ger högre smältpunkt.
Tabellen stämmer alltså.
Ok eftersom ädelgas har inga ledning elektron är det tvärtom för ädelgas?
Nej, det ser ut som om mitt arbetsminne inte riktigt räcker till när man behöver scrolla. Dr. G har alldeles rätt.
Van der Waalsbindnigens styrka beror på arean av de saker den håller ihop. Större atomer ger starkare bindning ger högre smältpunkt.
smaragdalena skrev :Van der Waalsbindnigens styrka beror på arean av de saker den håller ihop. Större atomer ger starkare bindning ger högre smältpunkt.
Men vist cesium är större än lithium? Men den har smältpunkten på bara 669 istället för 1342 fö lithium?
Ja, för metallerna gäller att mindre atomer ger högre smält-och kokpunkt. Man kan anse att metallen är uppbyggd av metalljoner och elektroner. Ju närmare laddade saker kommer varandra, desto starkare blir krafterns som håller ihop dem och desto mer måste atomerna vibrera för att kunna lossna från varann, d v s desto högre blir smält-och kokpunkt.
Ok jag tror jag är med...
Kommentarer om svenska: Det heter ett mysterium, inte bara mysteri. Smälta handlar alltid om att förändra från fast till flytande, så man kan inte smälta en gas.
fast => flytande smälta flytande => fast stelna eller frysa
flytande => gas koka gas => flytande kondensera
fast <=> gas sublimera (ja, det heter likadant åt båda hållen)




