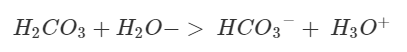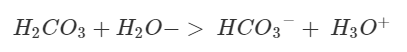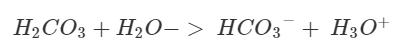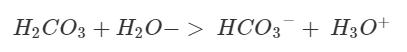Läsk med pH 5: Titrerkruvor

Jag har fastnat på c-uppgiften
pka för kolsyra= 6,32
Ka för kolsyra = 10^(-6,32)
Vi ville ha pH 5 alltså konc 10^-5 på oxoniumjonerna
Men då får jag två okända, hur ska jag ta reda på koncentrationen av HCO3 - för att sedan kunna få reda på konc för kolsyran som jag vill åt?
Samma koncentration av H3O+ som HCO3 :D
Aloosher skrev:Samma koncentration av H3O+ som HCO3 :D
Aha okej, hur vet jag det?
linnea.matte skrev:Aloosher skrev:Samma koncentration av H3O+ som HCO3 :D
Aha okej, hur vet jag det?
Beklagar för väldigt sent svar, hade inte på notiser på denna tråd, men i alla fall hoppas jag att det inte är för sent: 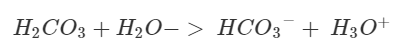
Där har du din kemiska jämvikt, för varje H3O+ måste det finnas en HCO3- enligt jämvikten. Om det finns 5 H3O+ betyder det att 5 styck H2CO3 och 5 styck H2O har reagerat och därmed måste det finnas 5 HCO3- samt 5 H3O+ som vi sa i början.
Aloosher skrev:linnea.matte skrev:Aloosher skrev:Samma koncentration av H3O+ som HCO3 :D
Aha okej, hur vet jag det?
Beklagar för väldigt sent svar, hade inte på notiser på denna tråd, men i alla fall hoppas jag att det inte är för sent:
Där har du din kemiska jämvikt, för varje H3O+ måste det finnas en HCO3- enligt jämvikten. Om det finns 5 H3O+ betyder det att 5 styck H2CO3 och 5 styck H2O har reagerat och därmed måste det finnas 5 HCO3- samt 5 H3O+ som vi sa i början.
Okej så då får man anta att Volymen i burken också är den samma så stämmer det att alla har samma konc då förhållandet är 1:1. Men det är egentligen inte ett helt rätt antagande.
linnea.matte skrev:Aloosher skrev:linnea.matte skrev:Aloosher skrev:Samma koncentration av H3O+ som HCO3 :D
Aha okej, hur vet jag det?
Beklagar för väldigt sent svar, hade inte på notiser på denna tråd, men i alla fall hoppas jag att det inte är för sent:
Där har du din kemiska jämvikt, för varje H3O+ måste det finnas en HCO3- enligt jämvikten. Om det finns 5 H3O+ betyder det att 5 styck H2CO3 och 5 styck H2O har reagerat och därmed måste det finnas 5 HCO3- samt 5 H3O+ som vi sa i början.
Okej så då får man anta att Volymen i burken också är den samma så stämmer det att alla har samma konc då förhållandet är 1:1. Men det är egentligen inte ett helt rätt antagande.
Vad menar du? Antagandet är helt korrekt?
Volymen i burken har inget med saken att göra, det enda vi förutsätter är att H2CO3 är den begränsande delen och att det finns gott om vatten (vilket det gör när man säger att något är i en vattenlösning)
Aloosher skrev:linnea.matte skrev:Aloosher skrev:linnea.matte skrev:Aloosher skrev:Samma koncentration av H3O+ som HCO3 :D
Aha okej, hur vet jag det?
Beklagar för väldigt sent svar, hade inte på notiser på denna tråd, men i alla fall hoppas jag att det inte är för sent:
Där har du din kemiska jämvikt, för varje H3O+ måste det finnas en HCO3- enligt jämvikten. Om det finns 5 H3O+ betyder det att 5 styck H2CO3 och 5 styck H2O har reagerat och därmed måste det finnas 5 HCO3- samt 5 H3O+ som vi sa i början.
Okej så då får man anta att Volymen i burken också är den samma så stämmer det att alla har samma konc då förhållandet är 1:1. Men det är egentligen inte ett helt rätt antagande.
Vad menar du? Antagandet är helt korrekt?
Volymen i burken har inget med saken att göra, det enda vi förutsätter är att H2CO3 är den begränsande delen och att det finns gott om vatten (vilket det gör när man säger att något är i en vattenlösning)
Jo volymen har något med det att göra då volymen hör ihop med vad koncentrationen är för något. (n/V= c)
Att substansmängden är den samma gör inte nödvändigtvis att koncentrationen är den samma.
linnea.matte skrev:Aloosher skrev:linnea.matte skrev:Aloosher skrev:linnea.matte skrev:Aloosher skrev:Samma koncentration av H3O+ som HCO3 :D
Aha okej, hur vet jag det?
Beklagar för väldigt sent svar, hade inte på notiser på denna tråd, men i alla fall hoppas jag att det inte är för sent:
Där har du din kemiska jämvikt, för varje H3O+ måste det finnas en HCO3- enligt jämvikten. Om det finns 5 H3O+ betyder det att 5 styck H2CO3 och 5 styck H2O har reagerat och därmed måste det finnas 5 HCO3- samt 5 H3O+ som vi sa i början.
Okej så då får man anta att Volymen i burken också är den samma så stämmer det att alla har samma konc då förhållandet är 1:1. Men det är egentligen inte ett helt rätt antagande.
Vad menar du? Antagandet är helt korrekt?
Volymen i burken har inget med saken att göra, det enda vi förutsätter är att H2CO3 är den begränsande delen och att det finns gott om vatten (vilket det gör när man säger att något är i en vattenlösning)
Jo volymen har något med det att göra då volymen hör ihop med vad koncentrationen är för något. (n/V= c)
Att substansmängden är den samma gör inte nödvändigtvis att koncentrationen är den samma.
Jo för att substansmängden är densamma i samma lösning, vilket innebär samma koncentration
:D
Jo för att substansmängden är densamma i samma lösning, vilket innebär samma koncentration
Bara om det är samma volym.