Lewisstrukturer: NO2
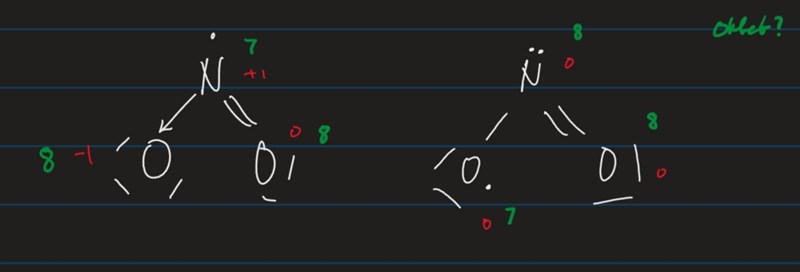
Hej, varför är följande lewisstruktur till höger för NO2 inte rätt? Jag har googlat och vänster är rätt.
Röda siffror är formella laddningar och gröna är antalet valenselektroner. Båda är lika dåliga när det kommer till oketetregeln, men högra är bättre för de formella laddningarna.
Det är ju en resonansstruktur, så jag skulle säga att båda figurerna bidrar till den sanna strukturen. Syre är mer elektronegativt än kväve så det är möjligt att man får en energisänkning av att placera den oparade elektronen på kvävet istället, dvs så man har högre elektrontäthet runt syrena. Men ingen av bilderna är ju helt sann, utan det är en blandning.
Men hur vet du att det är en blandning mellan de?
Jag råkade hitta en uppgift på en gammal tenta och där står faktiskt lewisstrukturen till vänster i facit, inte den till höger! Det är så konstigt; den till höger är objektivt bättre.
Vad har facit för argument?
Inga alls. Jag mailade även min lärare och han svarade inte varför. Han sa inte ens något om det faktum att högra alternativet är bättre enligt formell laddning.



