Massprocent
 Hej! Har stått stilla på följande uppgift väldigt länge nu och kommer ingen vart, frågan känns så lång och slingrig att man inte vet vad man ska göra och i vilken ordning. Är verkligen tacksam för all hjälp!
Hej! Har stått stilla på följande uppgift väldigt länge nu och kommer ingen vart, frågan känns så lång och slingrig att man inte vet vad man ska göra och i vilken ordning. Är verkligen tacksam för all hjälp!
Har du ngn tanke på hur du vill angripa problemet?
Alltså jag har prövat på lite olika sätt men aldrig kommit nån vart. Tänkte skriva reaktionsformel för järnet och svavelsyran men det gav mig inte så mycket jag kunde räkna på eftersom att msn inte vet substansmängden för enbart järnet i den metallbiten. Som jag förstått finns det fler ämnen i metallbiten, utöver järn, men som inte nämns, så då blir det lite svårt att ta reda på mur mycket järn som faktiskt finns för att sedan komma vidare.
Då tar vi det från början. Vad händer med järnet o svavelsyran?
Järnet oxideras till Fe2+ och svavelsyran reduceras till vätgas och sulfatjoner?
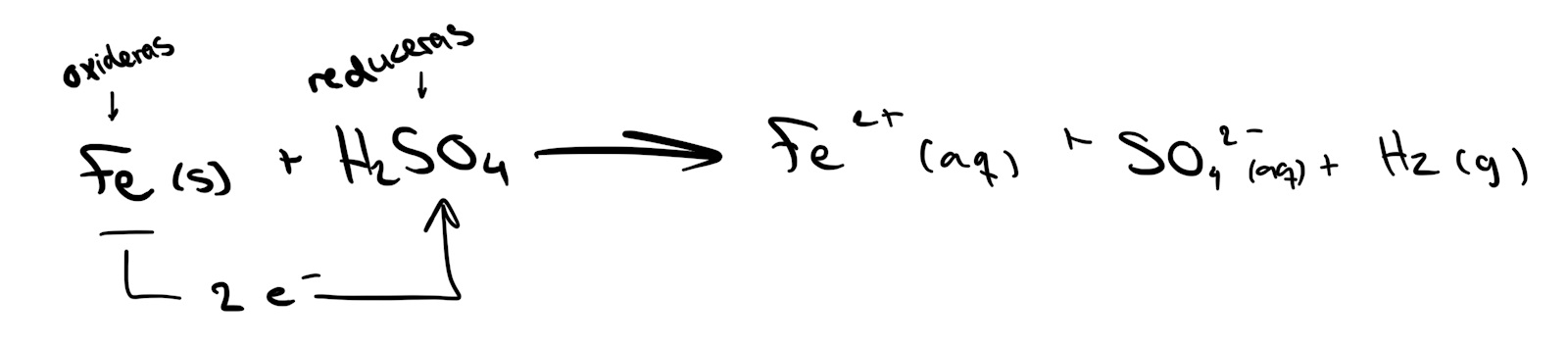
OK. Vet vi hur mkt svavelsyra vi använder?
Hallååå
I uppgiften anger de bara svavelsyran koncentration, säger mig inte så mycket om hur mycket som faktiskt reagerar.
Så då är väl svaret på min fråga nej.
Tycker du att vi då kan dra slutsatsen att allt järn är Fe2+, dvs svavelsyran är i överskott?
Jag tänker ändå att det kan stämma. Men finns ingen större grund för det i uppgiften.
Så du säger nej?
Ett osäkert nej men det är ett nej.
Så då har vi situationen att man har ett metallstycke med okänd halt av järn. Sen behandlar man det med svavelsyra så att bara en okänd del av järnet blir Fe2+. Är det så du uppfattar det?
Yes
Då har vi två okända variabler o inga ekvationer. Således olösbart!
Så uppgiften är olösbar, eller är det min tolkning av uppgiften som är det?
Läs den 2a meningen mkt långsamt fram till "titrerades" o tänk efter!
Borde man tolka det som att allt järn reagerade?
Ja! Så vill du ändra ditt svar på #9 ovan?
Nejdå! Den går visst att lösa.
Så här skulle jag ge mig på den:
- Vad är förhållandet mellan manganatjoner och järn(II)joner, när de reagerar i sur lösning?
- Vi vet hur mycket kaliumpermanganat som förbrukats.
- Då kan vi räkna ut substansmängden järn givet förhållandet i #1.
- Detta ger oss massan järn.
- Vi vet vad metallstycket vägde.
Ungefär så … Kommer du vidare?
Jag loggar ut o låter sic köra vidare
Svavelsyran är i överskott och allt järn reagerar.
KlmJan skrev:Svavelsyran är i överskott och allt järn reagerar.
Svavelsyran har ingen betydelse för uträkningen. Den är för att lösa upp järnstycket, ge dig järn(II)joner i sur lösning. Ett stickspår som inte hjälper dig.
Kika på mitt svar och prova därifrån. Fråga på, så försöker jag hjälpa till på vägen.
Jaa, jag insåg detta när jag läste ditt svar, håller på att försöka ta mig fram just nu, återkommer när jag kommit en bit på vägen :)
KlmJan skrev:Jaa, jag insåg detta när jag läste ditt svar, håller på att försöka ta mig fram just nu, återkommer när jag kommit en bit på vägen :)
Lycka till! Det blir säkert bra.
Här är massan jag kommit fram till men den känns lite väl låg för den totala massan.
 Ett annat problem är att jag inte skrivit hela reaktionsformeln. Vet inte riktigt vad man ska skriva som produkter.
Ett annat problem är att jag inte skrivit hela reaktionsformeln. Vet inte riktigt vad man ska skriva som produkter.
Så här ser nettoreaktionen ut:
MnO4- (aq) + 5Fe2+ (aq) + 8H+ (aq) → 5Fe3+ (aq) + Mn2+ (aq) + 4H2O (l)
Du ser ut att ha en faktor x10 för låg substansmängd järn, men siffrorna ser rätt ut. Fem gånger n(manganat) måste bli mer än du har.
Ahh ... Du har dividerat med två istället för att multiplicera med fem. Då blir siffrorna lika, förutom magnituden då.
Kikar du på reaktionen ovan så går det åt fem järn för varje manganat.
Hmm, var kom vätet ifrån? Gissningsvis från svavelsyran tidigare, men hur skulle man isf balansera allt detta? Med OT eller ta ett grundämne i taget? Nu minns jag inte exakt hur detta gick till men det fanns väl någon metod där man i slutet la till väte och vatten för att typ balansera resten av syret som ännu inte var balanserat efter allt annat. Är det därifrån de tillkommer för de finns ju i lösningarna, men försöker första hur de kommer in i reaktionen.
Eftersom det inte står något så får man anta att det är en vanlig titrering och att det finns massor av vätejoner i överskott från svavelsyran. 2M är rätt koncentrerad så även en liten mängd är mer än tillräckligt för de mängder du har.
Det man behöver veta är att förhållandet är 1:5 mellan de intressanta jonerna.
Sedan har jag inte jättekoll på hur du förväntas ställa upp och redovisa, men räknandet kan jag klara.
 Liiite off i avrundningen, i facit stod det 79,78%. Eddan har jag inte helt förstått hur balanseringen gick till.
Liiite off i avrundningen, i facit stod det 79,78%. Eddan har jag inte helt förstått hur balanseringen gick till.
Jag får ca 79,85 och skulle ha svarat 79,9 massprocent. (Svavelsyrans koncentration är inte intressant.) Kanske räknar facit med någon annan molmassa någonstans?
Sedan blir det järn(III)joner på produktsidan.
Vad gäller balanseringen så förändras inte substansmängderna manganat eller järn. Du har samma värden för mangan- och järn(III)joner som på reaktantsidan.
Vad gäller balanseringen så förändras inte substansmängderna manganat eller järn. Du har samma värden för mangan- och järn(III)joner som på reaktantsidan.
Jo, det förstår jag, nu är den redan balansrad liksom, men hade den uppgiften kommit på kursprovet hade jag ju inte haft någon aning om att det var väte och vatten med i reaktionen också, eller att det blev Fe(III) joner sedan.
På tal om Fe(III) joner, då har den lämnat ifrån sig ytterligare en elektron till manganen så den kan bli till en jon Mn2+. Egentligen har ju den jonen 7+ i elektronladdning, men för att bli 2+ måste den plocka 5 elektroner från någonstans, därmed de 5 järn(II)jonerna. Sedan för att det ska finnas syre på produktsidan tillsätter man vatten i reaktionen för att de är ju ändå läsningar så vatten finns där, 4 för att det är 4 syreatomer på reaktantsidan, och sedan balanseras vätet i vattnet med ytterligare 8 vätejoner på reaktantsidan.
Facit tyckte jag va väldigt svårt att förstå, speciellt eftersom att de började med att skriva reaktionsformeln för metallen i svavelsyran, men skrev in någon random massa på järnet man inte får från uppgiften, och hur den massan uppkom förklarandes heller aldrig.
När facit räknar på masshalten skriver de först att det är substansmängderna som ska divideras, men divideras sedan ändå massorna, och skriver att massan järn är 0,2018 g


