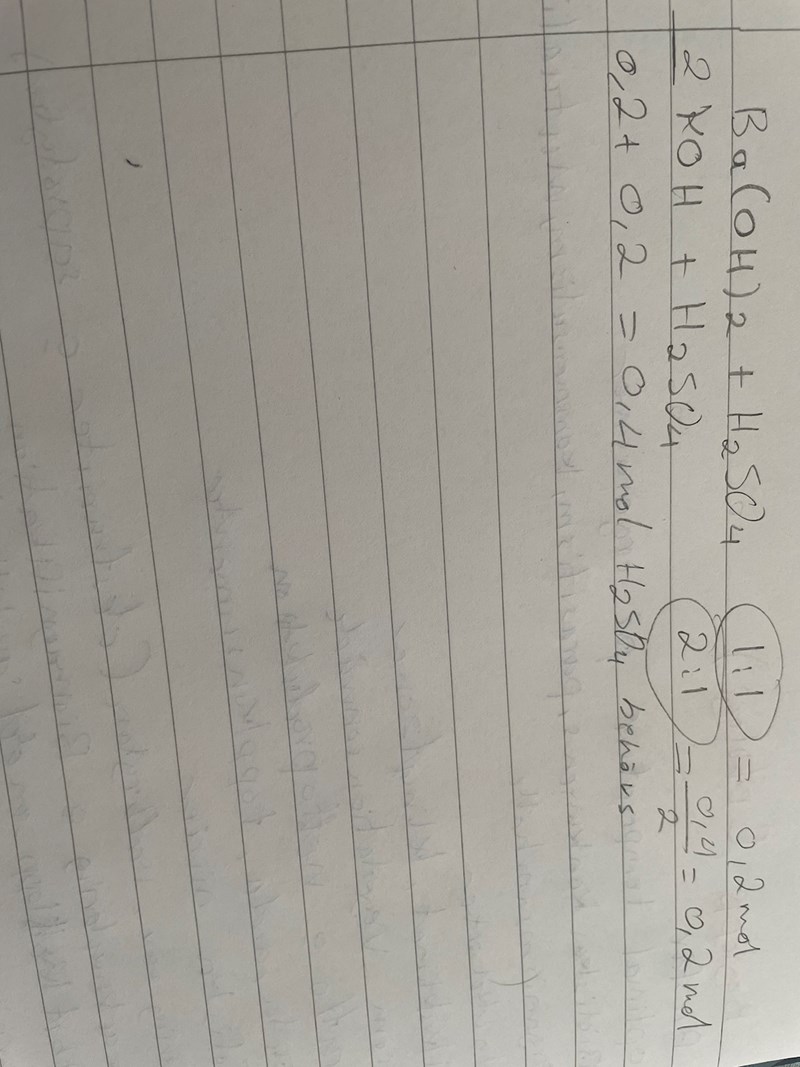Neutralisera blandningen
Hej!
Jag håller på med en fråga som lyder så här:
"Man har en blandning av 0,2 mol bariumhydroxid och 0,4 mol kaliumhydroxid. Vilken mängd svavelsyra (i mol) behövs för att neutralisera blandningen?"
För att neutralisera en blandning så behöver koncentrationen av en syra och en bas vara lika stor. Både bariumhydroxid och kaliumhydroxid är ju baser och deras koncentration tillsammans blir då 0,6 mol, så därför tänkte jag att det behövs 0,6 mol svavelsyra för att neutralisera blandningen. Men detta är tydligen fel, för att på facit står det att svaret ska bli 0,4 mol. Varför då? Varför går det inte att tänka som jag har gjort?
Tack på förhand!
Hur kan Ba(OH) + H2SO4 bli 0,2 mol? Borde det inte bli 0,4 mol eftersom 0,2 mol Ba(OH) + 0,2 mol H2SO4 = 0,4 mol?
Hur många mol hydroxidjoiner finns det i 1 mol bariumhydroxid? Hur många mol hydroxidjoner finns det i 0,2 mol bariumhydroxid?
Hur många mol hydroxidjoiner finns det i 1 mol natriumhydroxid? Hur många mol hydroxidjoner finns det i 0,4 mol natriumhydroxid?
Därefter är det tags att addera substansmängderna av hydroxidjoner.
Molförhållandet är 1:1 och då borde substansmängderna i det fallet vara lika, jag dividerade med 2 när det handlade om KOH därför att molförhållandet är 2:1 sedan adderar du substansmängderna och då får i svar 0,4 mol
Aboud skrev:Molförhållandet är 1:1 och då borde substansmängderna i det fallet vara lika, jag dividerade med 2 när det handlade om KOH därför att molförhållandet är 2:1 sedan adderar du substansmängderna och då får i svar 0,4 mol
Vad är det för molförhållande du menar?
Smaragdalena skrev:Hur många mol hydroxidjoiner finns det i 1 mol bariumhydroxid?
1 mol/dm3? Är enheten korrekt?
Hur många mol hydroxidjoner finns det i 0,2 mol bariumhydroxid?
0,2 mol/dm3?
Hur många mol hydroxidjoiner finns det i 1 mol natriumhydroxid?
1 mol/dm3?
Hur många mol hydroxidjoner finns det i 0,4 mol natriumhydroxid?
0,4 mol/dm3?
Därefter är det tags att addera substansmängderna av hydroxidjoner.
Men då blir det väll 0,6 mol? Eftersom 0,2 + 0,4 = 0,6?
-----------------------------------------
Men det känns ändå som att jag har gjort helt fel....
karisma skrev:Smaragdalena skrev:Hur många mol hydroxidjoiner finns det i 1 mol bariumhydroxid?
1 mol/dm3? Är enheten korrekt?
Nej, 2 mol. Formeln för mariumhydroxid är Ba(OH)2 (bariumjonen har ju laddningen +2).
Hur många mol hydroxidjoner finns det i 0,2 mol bariumhydroxid?
0,2 mol/dm3?
Nej, 0,4 mol.
Hur många mol hydroxidjoiner finns det i 1 mol natriumhydroxid?
1 mol/dm3?
Nej, 1 mol.
Hur många mol hydroxidjoner finns det i 0,4 mol natriumhydroxid?
0,4 mol/dm3?
Nej, 0,4 mol.
Därefter är det tags att addera substansmängderna av hydroxidjoner.
Men då blir det väll 0,6 mol? Eftersom 0,2 + 0,4 = 0,6?
Ja, om det hade varit 0,2 och 0,4 mol.
-----------------------------------------
Men det känns ändå som att jag har gjort helt fel....
Ja, se ovan.
Smaragdalena skrev:karisma skrev:Smaragdalena skrev:Hur många mol hydroxidjoiner finns det i 1 mol bariumhydroxid?
1 mol/dm3? Är enheten korrekt?
Nej, 2 mol. Formeln för mariumhydroxid är Ba(OH)2 (bariumjonen har ju laddningen +2).
Så (nu tänker jag mer allmänt) står alltid den nedsänkta siffran för hur många mol det finns av en atom i ett visst ämne? Som t.ex. nu när det stod Ba(OH)2 står 2an för att det finns 2 mol OH? Nu vet jag att det inte står Ba(OH)3 men om det hade stått så hade det då betytt att det finns 3 mol OH?
Hur många mol hydroxidjoner finns det i 0,4 mol natriumhydroxid?
Hur är det menat att man ska räkna ut det här? Ska man bara kolla på formeln för natriumhydroxiden och kolla hur många OH det finns? Eller finns det någon speciell formel man kan använda sig av för att räkna ut hur många mol hydroxidjoner det finns i en bas?
karisma skrev:Smaragdalena skrev:karisma skrev:Smaragdalena skrev:Hur många mol hydroxidjoiner finns det i 1 mol bariumhydroxid?
1 mol/dm3? Är enheten korrekt?
Nej, 2 mol. Formeln för mariumhydroxid är Ba(OH)2 (bariumjonen har ju laddningen +2).
Så (nu tänker jag mer allmänt) står alltid den nedsänkta siffran för hur många mol det finns av en atom i ett visst ämne? Som t.ex. nu när det stod Ba(OH)2 står 2an för att det finns 2 mol OH? Nu vet jag att det inte står Ba(OH)3 men om det hade stått så hade det då betytt att det finns 3 mol OH?
Ja. Vi kan ju ta Al(OH)3 som exempel istället.
Hur många mol hydroxidjoner finns det i 0,4 mol natriumhydroxid?
Hur är det menat att man ska räkna ut det här? Ska man bara kolla på formeln för natriumhydroxiden och kolla hur många OH det finns? Eller finns det någon speciell formel man kan använda sig av för att räkna ut hur många mol hydroxidjoner det finns i en bas?
1 mol NaOH innehåller 1 mol hydroxidjoner, så 0,4 mol NaOH innehåller 0,4 mol hydroxidjoner.
Man kan säga att det finns en "osynlig nedsänkt etta" för OH- i NaOH, om man vill.
Okej då förstår jag, tack för hjälpen!