Övergångar och emissionslinjer
Jag har kört fast på denna uppgiften och förstår inte riktigt hur jag ska lösa denna.
”En atom har energitillstånden E1= 0,00 eV, E2= 3,00 eV samt E3= 5,00 eV.
a/ Hur många linjer observeras i absorptionspektrat från denna atom och vilka är de?
b/ Hur många linjer observeras i emissionsspektrat från denna atom och vilka är det?
Totalt söks fem övergångar. Ange i samtliga fall vilken energi (i eV) samt våglängd (i nm) övergången motsvarar.”
Har förstått att jag kan använda Rydbergs formel på något sett men en vägledning skulle uppskattas.
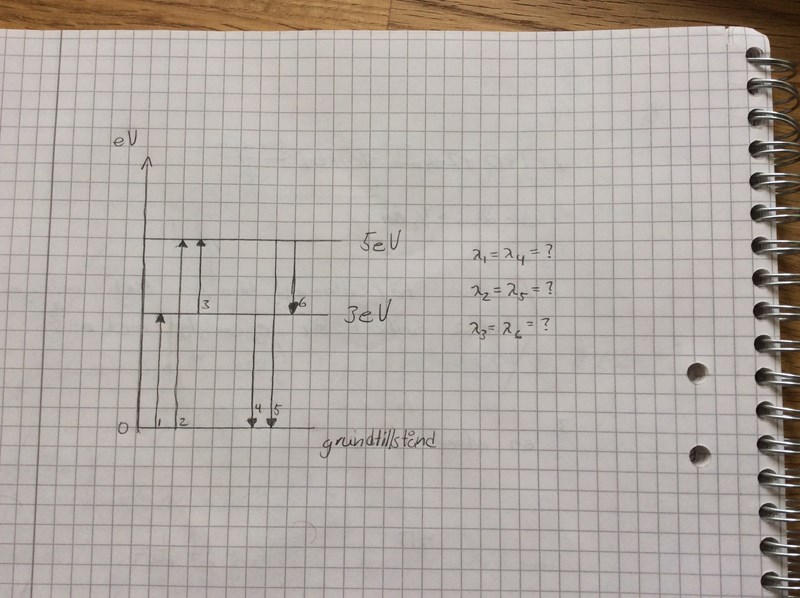
Har du ritat upp ett diagram över energinivåerna?
Smaragdalena skrev:Har du ritat upp ett diagram över energinivåerna?
Nej, tyvärr inte. Läste den här kursen för någon år sedan och haft den som släpande tenta så försöker ta tag i den nu men har glömt det mesta..
Tog bort onödig fetstil /Smaragdalena, moderator
Då behöver du repetera energinivådiagram. Rita ett och lägg upp bilden här, så kan vi resonera vidare.
Borde det inte då finnas 6 övergångar och inte 5 som uppgiften säger?