Oxidationstal i organisk kemi
När man räknar på oxidationstal i organisk kemi räknar man väl enbart på de kol där något händer under reaktionen! När man sedan ska jämföra reaktantens oxidationstal med produktens jämför man då summan av reaktantens oxidationstal med summan av produktens oxidationstal eller jämför man det ena kolet med det andra? Och om båda har ökat är det oxidation och om båda minskat så är det reduktion om ingen förändrats har inget hänt och om den ena förändrats men ej den andra så är det oxidation/inte?
tack på förhand
Man tittar bara på de kol som reagerar - de andra är ointressanta. Om oxidationstalet ökar för ett kol, så ar det oxiderats. Om oxidationstalet minskar för ett kol, så har det reducerats. Om någonting har oxiderats, så måste något annat (ett oxidationsmedel) ha reducerats.
Smaragdalena skrev:Man tittar bara på de kol som reagerar - de andra är ointressanta. Om oxidationstalet ökar för ett kol, så ar det oxiderats. Om oxidationstalet minskar för ett kol, så har det reducerats. Om någonting har oxiderats, så måste något annat (ett oxidationsmedel) ha reducerats.
Men vad händer om båda ökar, båda minskar eller en minskar och en ökar? Ska de kol man tittar minska och öka med lika mycket?
tack på förhand
Om något oxideras så måste något annat reduceras. Om det som reduceras inte finns i den intressanta molekylen kan man t ex markera att man behöver tillsätta ett oxidationsmedel. Ett sätt att markera det är att skriva (ox) eller något liknande ovanför reaktionspilen.
Smaragdalena skrev:Om något oxideras så måste något annat reduceras. Om det som reduceras inte finns i den intressanta molekylen kan man t ex markera att man behöver tillsätta ett oxidationsmedel. Ett sätt att markera det är att skriva (ox) eller något liknande ovanför reaktionspilen.
Men vad händer om båda/eller ännu fler oxidationstalen i produkten ökar, båda minskar eller en minskar och en ökar? Ska de kol man tittar minska och öka med lika mycket
Men vad händer om båda/eller ännu fler oxidationstalen i produkten ökar, båda minskar eller en minskar och en ökar? Ska de kol man tittar minska och öka med lika mycket
Nej, för tredje gången bara i den här tråden: Man använder sig av ett oxidationsmedel för att oxidera det intressanta ämnet.
Smaragdalena skrev:Men vad händer om båda/eller ännu fler oxidationstalen i produkten ökar, båda minskar eller en minskar och en ökar? Ska de kol man tittar minska och öka med lika mycket
Nej, för tredje gången bara i den här tråden: Man använder sig av ett oxidationsmedel för att oxidera det intressanta ämnet.
Ja, det vet jag! Men min fråga gäller angående uträkningen av oxidationstalet! Alltså om man har något som reagerar (med ett oxidationsmedel) och det är exempelvis två kol i reaktanten som är med och reagerar! Båda dessa kol har innan reaktionen oxidationstalen -1! I Produkten som bildas har ena kolet oxidationstalet -2 och det andra 0! Ska man då slå ihop oxidationstalet i reaktanten som då blir -2 och jämföra med produktens oxidationstal som också är -2 och komma fram till att det inte skett en oxidation eller reduktion! Eller ska man jämföra varje kol för sig och komma fram till att det skett en reduktion?
tack på förhand
Skriv vad det är för reaktion du håller på med! Det är meningslöst att försöka gissa vad det är du menar. Vi kan inte ge dig bra svar om vi inte vet vad det handlar om.
Smaragdalena skrev:Skriv vad det är för reaktion du håller på med! Det är meningslöst att försöka gissa vad det är du menar. Vi kan inte ge dig bra svar om vi inte vet vad det handlar om.
Man ska beräkna oxidationstal på reaktion 10 och 12 och jämföra dem! Jag räknade på de två kolen vid dubbelbindningen och fick -1 på vardera och sedan räknade jag vid samma två kol sedan och fick 0 på ena och -2 på andra (då svavel räknas som syre vid beräkning av oxidationstal) jag vet inte hur jag ska jämför och inte heller om jag räknat rätt!
tack på förhand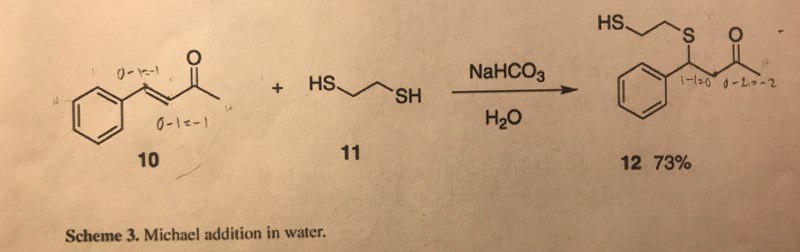
Bild 10 och 12 föreställer inte reaktioner. Hela bilden föreställer en reaktion mellan två reaktanter (10 och 11) där det bildas en produkt (12).
Det ena kolet har oxiderats, det andra har reducerats.
(då svavel räknas som syre vid beräkning av oxidationstal)
Vad menar du med det? Svavel kan ha alla möjliga oxidationstal mellan -II och +VI. Om du menar att svavel har högre elektronegativitet än kol stämmer det, men skillnaden är väldigt liten (2,58 respektive 2,55).
Kan du lägga in en bild av HELA uppgiften! Står det verkligen att man skall ta reda på oxidationstalen? Oxidationstal är mer användbara i oorganisk kemi än i organisk.
Smaragdalena skrev:Bild 10 och 12 föreställer inte reaktioner. Hela bilden föreställer en reaktion mellan två reaktanter (10 och 11) där det bildas en produkt (12).
Det ena kolet har oxiderats, det andra har reducerats.
(då svavel räknas som syre vid beräkning av oxidationstal)
Vad menar du med det? Svavel kan ha alla möjliga oxidationstal mellan -II och +VI. Om du menar att svavel har högre elektronegativitet än kol stämmer det, men skillnaden är väldigt liten (2,58 respektive 2,55).
Kan du lägga in en bild av HELA uppgiften! Står det verkligen att man skall ta reda på oxidationstalen? Oxidationstal är mer användbara i oorganisk kemi än i organisk.
Det stod i uppgiften att vi skulle räkna svavel som syre i denna uppgift (det kanske bara är för att vi ska förenkla det). Har tyvärr inte bild på hela uppgiften men vi jobbar med oxidationstal trots att vi jobbar med organisk kemi och jag vet att frågan var att beräkna oxidationstal på molekyl 10 och 12 och därefter jämföra det.
Tack på förhand
Smaragdalena skrev:Bild 10 och 12 föreställer inte reaktioner. Hela bilden föreställer en reaktion mellan två reaktanter (10 och 11) där det bildas en produkt (12).
Det ena kolet har oxiderats, det andra har reducerats.
(då svavel räknas som syre vid beräkning av oxidationstal)
Vad menar du med det? Svavel kan ha alla möjliga oxidationstal mellan -II och +VI. Om du menar att svavel har högre elektronegativitet än kol stämmer det, men skillnaden är väldigt liten (2,58 respektive 2,55).
Kan du lägga in en bild av HELA uppgiften! Står det verkligen att man skall ta reda på oxidationstalen? Oxidationstal är mer användbara i oorganisk kemi än i organisk.
Om ett kol har oxiderats och ett reducerats vad har då skett totalt?
Om ett kol har oxiderats och ett reducerats vad har då skett totalt?
Det är ointressant.


