Protonering och deprotonering av Zn bundet vatten
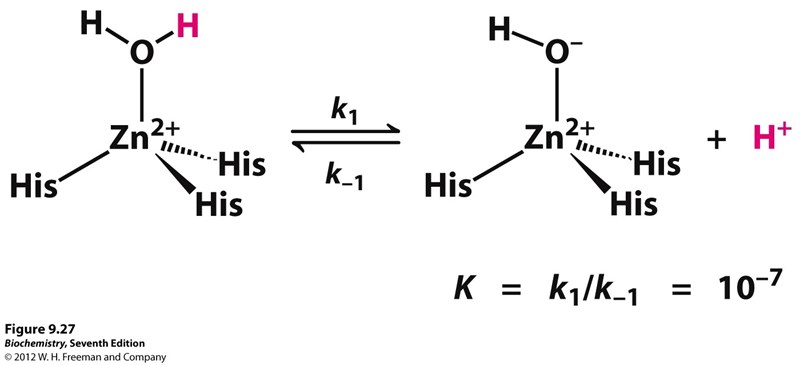
Man skriver i boken att:
“The reverse reaction - the protonation of the Zn bound OH- is limited by the rate of proton diffusion. Protons diffuse very rapidly within second order rate constants near 1011 / (M*s). Thus the backward reaction constant k-1 must be less than 1011 / (M*s). Because the equilibrium constant K = k1 / k-1 and k-1 < 10-11 then k1 is equal to or less than 104/s. In other words the rate of proton diffusion limits the rate of proton release to <104 /s for a group with pKa 7. However if CO2 is hydrated at 106 /s then every step in the mechanism must take place at least this fast.”
Vad syftar second order på där man använder det, hur vet man att det är det och vilka är reaktanterna?
Varför måste k-1 vara mindre än 1011?
Den sista meningen - vad menar man med att varje steg måste ske i hastigheten av 106 /s?
Sedan säger man att K = 10-7 pga pKa = 7. Jag är med på att pKa här blir 7 för det Zn bundna vattnet - men jag är inte med på hur detta kommer in i en ekvation för K - vart är sambandet?

