Reaktionsmekanism
Hej, jag förstår inte riktigt reaktionsmekanism. Jag vet att man ritar pilen från bindningen till atomen då bindningar bryts och att man ritar pilen från laddningen till atomen då bindningar skapas. Jag förstår dock inte riktigt hur man använder detta i uppgifter. Hur vet man om man ska skriva reaktionen i två led och kan man max ha tre pilar i ett led?
Tack på förhand
Oklart vad det är du behöver hjälp med. Skulle du kunna förtydliga hur du menar? Något konkret exempel i en uppgift kanske?
Teraeagle skrev:Oklart vad det är du behöver hjälp med. Skulle du kunna förtydliga hur du menar? Något konkret exempel i en uppgift kanske?
Jag förstår inte riktigt hur man vet att 1. om reaktionen är SN1 eller SN2 och följaktligen vet jag inte om reaktionen ska ritas i ett eller två led. 2. Hur många pilar kan man rita i ett steg? Är det så att man max kan rita tre pilar i varje steg?
Tack på förhand
Vad är det du för pilar du skriver om?
Ge gärna ett konkret exempel så kan vi diskutera utifrån det. Är problemet att du inte vet vid vilka typer av reaktioner de två reaktionerna sker eller att du inte kan säga vad som är vad ifall någon ritar ut mekanismen för en reaktion?
Teraeagle skrev:Vad är det du för pilar du skriver om?
Ge gärna ett konkret exempel så kan vi diskutera utifrån det. Är problemet att du inte vet vid vilka typer av reaktioner de två reaktionerna sker eller att du inte kan säga vad som är vad ifall någon ritar ut mekanismen för en reaktion?
facit:
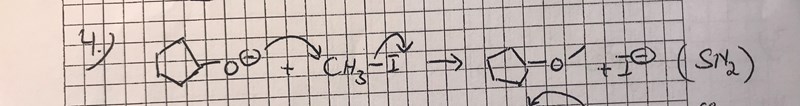
frågan: (ange reaktionsmekanismen och avgör om reaktionerna är SN1 eller SN2)
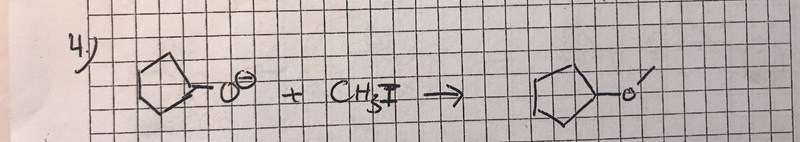
I ett fall som detta förstår jag inte hur jag vet att "elektronerna som förflyttas från syre till kolet" och "elektroner som förflyttas till jod" ska vara i ett steg alltså en SN2 reaktion och därför har jag svårt att avgöra om ytterligare led bör ritas till. Jag förstår inte heller hur man vet hur många pilar som får ritas ut i ett steg (finns det något maxantal?) så att man på så sätt kan avgöra om flera led ska ritas. Avslutningsvis hur vet man att det exempelvis inte är så att joden tar elektronparet kolet och jod delar på, och följaktligen får kolet positiv laddning och dras åt syret. Varför lämnas först elektroner över till kolet?
Tack på förhand
Du vet att det är SN2 eftersom det är ett primärt kol (dvs en kolatom som inte binder till några andra kolatomer) som reagerar. De tre väteatomerna är ganska små och det finns ett utrymme för syret i fenolatjonen att komma nära kolatomen i metyljodiden.
Det var den ena viktiga faktorn. Det andra som är viktigt är att karbokatjonen CH3+ är väldigt instabil eftersom den är så liten, vilket gör att laddningen är väldigt koncentrerad på kolatomen och direkt ”limmar fast” jodatomen ifall den börjar avlägsna sig. Detta förhindrar effektivt en SN1-reaktion från att ske. Om man har en större, bulkigare karbokatjon (läs: ett tertiärt kol med bindning till alkylgrupper) så kan laddningen spridas ut över ett större område, delokaliseras, vilket ökar stabiliteten. Då kan jodatomen lämna helt och hållet utan att det kostar för mycket energi, vilket gör SN1-reaktionen mer sannolik. Det hade med andra ord varit en SN1-reaktion om det var C(CH3)3I som reagerade istället för CH3I.
Angående pilarna: I det här fallet börjar jodatomen omedelbart att avlägsnas när fenolatjonen börjar binda till kolatomen, så de sker samtidigt. Då är det rimligt att rita ut två pilar i samma bild. Om det ena steget skedde före det andra så ritar du istället ut två separata steg med varsin pil.
Teraeagle skrev:Du vet att det är SN2 eftersom det är ett primärt kol (dvs en kolatom som inte binder till några andra kolatomer) som reagerar. De tre väteatomerna är ganska små och det finns ett utrymme för syret i fenolatjonen att komma nära kolatomen i metyljodiden.
Det var den ena viktiga faktorn. Det andra som är viktigt är att karbokatjonen CH3+ är väldigt instabil eftersom den är så liten, vilket gör att laddningen är väldigt koncentrerad på kolatomen och direkt ”limmar fast” jodatomen ifall den börjar avlägsna sig. Detta förhindrar effektivt en SN1-reaktion från att ske. Om man har en större, bulkigare karbokatjon (läs: ett tertiärt kol med bindning till alkylgrupper) så kan laddningen spridas ut över ett större område, delokaliseras, vilket ökar stabiliteten. Då kan jodatomen lämna helt och hållet utan att det kostar för mycket energi, vilket gör SN1-reaktionen mer sannolik. Det hade med andra ord varit en SN1-reaktion om det var C(CH3)3I som reagerade istället för CH3I.
Angående pilarna: I det här fallet börjar jodatomen omedelbart att avlägsnas när fenolatjonen börjar binda till kolatomen, så de sker samtidigt. Då är det rimligt att rita ut två pilar i samma bild. Om det ena steget skedde före det andra så ritar du istället ut två separata steg med varsin pil.
Så det blir inte en SN1 reaktion om det leder till att karbokatjonen behöver vara instabil under en tid av reaktionen? Är karbokatjonen instabil när den är primär och sekundär? Men stabil då den är tertiär?
Tack på förhand
Det stämmer
Teraeagle skrev:Det stämmer
Men varför drar man dock pilen från minusladdningen till plusladdningen och inte tvärtom? Är det så att ma alltid gör det, eller?
Tack på förhand
Pilarna visar hur elektronerna rör sig.
Teraeagle skrev:Pilarna visar hur elektronerna rör sig.
Ok, så om man skulle dra från pluspilen visar man inte elektronernas rörelse och följaktligen måste pilen alltid dras från minusladdningen?
Tack på förhand
Menar du plusladdning när du skriver pluspil? I så fall har du rätt.
Kemiska reaktioner handlar alltid om hur elektroner förflyttar sig, så det är det man fokuserar på.
Teraeagle skrev:Menar du plusladdning när du skriver pluspil? I så fall har du rätt.
Kemiska reaktioner handlar alltid om hur elektroner förflyttar sig, så det är det man fokuserar på.
Oj, det blev lite fel. Jag menar plusladdning.
Teraeagle skrev:Om man har en större, bulkigare karbokatjon (läs: ett tertiärt kol med bindning till alkylgrupper) så kan laddningen spridas ut över ett större område, delokaliseras, vilket ökar stabiliteten. Då kan jodatomen lämna helt och hållet utan att det kostar för mycket energi, vilket gör SN1-reaktionen mer sannolik. Det hade med andra ord varit en SN1-reaktion om det var C(CH3)3I som reagerade istället för CH3I.
Vad menas med ett tertiärt kol med bidning till alkylgrupper är det inte det faktum att den är bunden till alkylgrupper som gör den tertiär? Varför sparar jodatomen energi genom att lämna ett tertiärt? Är det för att det hade krävts väldigt mycket energi för jod atomen att bryta sig loss från ett primärt kol eftersom det kolet desperat vill ha elektronerna de delar på för att vara stabil? Vad menar man även med att en elektron är stabil?
Tack på förhand
Ett tertiärt kol med bindning till alkylgrupper är ett kol som binder till tre andra kolvätekedjor (som inte innehåller några andra funktionella gruppen än möjligen dubbel- eller trippelbindningar, för du hade det inte varit alkylgrupper).
Varför sparar jodatomen energi genom att lämna ett tertiärt? Är det för att det hade krävts väldigt mycket energi för jod atomen att bryta sig loss från ett primärt kol eftersom det kolet desperat vill ha elektronerna de delar på för att vara stabil?
Vem har påstått att joidijonen (inte jodatomen) sparar energi? En tertiär karbokatjon är hyfsat stabil och kan ta hand om plusladdingen genom att den fördelas på hela jonen. En primär karbokatjon får en mer lokaliserad plusladdning, och det är inte förmånligt.
Vad menar man även med att en elektron är stabil?
Hittar du det uttrycket någonstans i den här frågan? Om inte, så bör du starta en ny tråd för den frågan.
Smaragdalena skrev:Ett tertiärt kol med bindning till alkylgrupper är ett kol som binder till tre andra kolvätekedjor (som inte innehåller några andra funktionella gruppen än möjligen dubbel- eller trippelbindningar, för du hade det inte varit alkylgrupper).
Varför sparar jodatomen energi genom att lämna ett tertiärt? Är det för att det hade krävts väldigt mycket energi för jod atomen att bryta sig loss från ett primärt kol eftersom det kolet desperat vill ha elektronerna de delar på för att vara stabil?
Vem har påstått att joidijonen (inte jodatomen) sparar energi? En tertiär karbokatjon är hyfsat stabil och kan ta hand om plusladdingen genom att den fördelas på hela jonen. En primär karbokatjon får en mer lokaliserad plusladdning, och det är inte förmånligt.
Vad menar man även med att en elektron är stabil?
Hittar du det uttrycket någonstans i den här frågan? Om inte, så bör du starta en ny tråd för den frågan.
(från tidigare i tråden) Då kan jodatomen lämna helt och hållet utan att det kostar för mycket energi, vilket gör SN1-reaktionen mer sannolik. Det hade med andra ord varit en SN1-reaktion om det var C(CH3)3I som reagerade istället för CH3I.
(från tidigare i tråden) Då kan jodatomen lämna helt och hållet utan att det kostar för mycket energi, vilket gör SN1-reaktionen mer sannolik. Det hade med andra ord varit en SN1-reaktion om det var C(CH3)3I som reagerade istället för CH3I.
Du frågade om en "stabil elektron". Nu svarar du med ett citat om en jodatom. Vad har det ena med det andra att göra?
Frågan är: Varför jodatomen kan lämna helt och hållet utan att det kostar för mycket energi (om det hade varit ett tertiärt kol det var bundet till)? Är detta för att ett tertiärt kol är så stabilt att det inte har så stort behov av elektronerna från joden och således kan joden lämna relativt enkelt?
Tack på förhand
En tertiär karbokatjon (inte kolatom) är tillräckligt stabil för att jodidjonen (inte jodatomen) skulle kunna lämna den, som Teraeagle skrev för tre dagar sedan i den här tråden.



