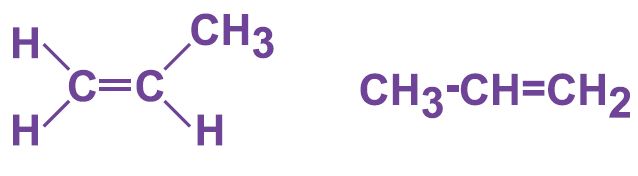
Reaktionsmekanism & isomeri
Hej! När det kommer till bromering av heptan, där en heptanmolekyl får reagera med Br2 och bilda (t.ex.) 2-bromo-heptan + HBr, undrar jag hur reaktionsmekanismen går till?
Är det så att ena bromidjonen Br- attraheras till H+ och "snor" den? (I just det ögonblicket när de har dessa laddningar)
Eller reagerar bromidjonen med en kolatom i heptan => intermediärt tillstånd där kolatomen har 5 bindningar => en väteatom frigörs för att stabilisera molekylen?
Dessutom... varför kan inte en sådan alken visa cis-trans-isomeri? 
Tack på förhand!
Dr.scofield skrev:Dessutom... varför kan inte en sådan alken visa cis-trans-isomeri?
Tack på förhand!
Det finns ingen substituent på kolet till vänster.
Dr.scofield skrev:Hej! När det kommer till bromering av heptan, där en heptanmolekyl får reagera med Br2 och bilda (t.ex.) 2-bromo-heptan + HBr, undrar jag hur reaktionsmekanismen går till?
Det kallas SR - radikalisk substitution och brukar ske vid uppvärmning eller initieras av andra radikaler eller UV-ljus.
Först bryts Br2 i två bromatomer Br* med en oparad elektron. En sådan radikal reagerar med t.ex. CH4 och tar en H-atom. Det bildas HBr och CH3* med en oparad elektron. CH3* reagerar med Br2 och tar upp en bromatom. Det bildas CH3Br och Br*. Och så fortsätter det - en kedjereaktion. Eventuellt avslutas kedjan om CH3* och Br* eller CH3* och CH3* reagerar med varandra eller med något annat i reaktionsblandningen.
MaKe skrev:Dr.scofield skrev:Dessutom... varför kan inte en sådan alken visa cis-trans-isomeri?
Tack på förhand!
Det finns ingen substituent på kolet till vänster.
Jag hänger med på reaktionsmekanismen, tack! Jag förstår dock inte riktigt detta med substituent... skulle du kunna förklara?
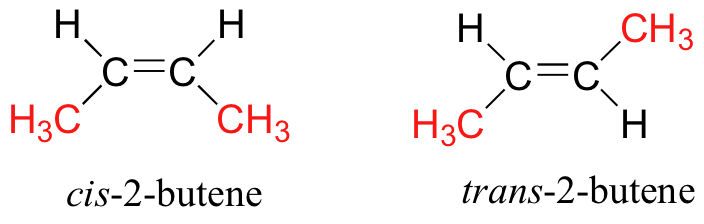
cis-2-buten - två metylgrupper är på samma sida av dubbelbindningen. trans-2-buten - två metylgrupper är på motsatta sidor om dubbelbindningen.
Propen - vad ska betecknas som cis- eller trans-? Blir de någon skillnad?