Silver löses i salpetersyra oxidationstal samt elektronövergångsmetoden (8:25)

Hej,
Har försök lösa 8:25 men lyckas inte. Förstår balanseringen med oxidationstalsmetoden men sen förstår jag inte hur kväveoxid och H2O bildas enligt faceit.
mvh,
valdemar
Hur långt har du kommit med oxidationstalsmetoden? Vilka oxidationstal har silver och kväve före respektive efter reaktionen? Uppgiften har varit snäll nog att ange vilka produkter som bildas vid reaktionen.
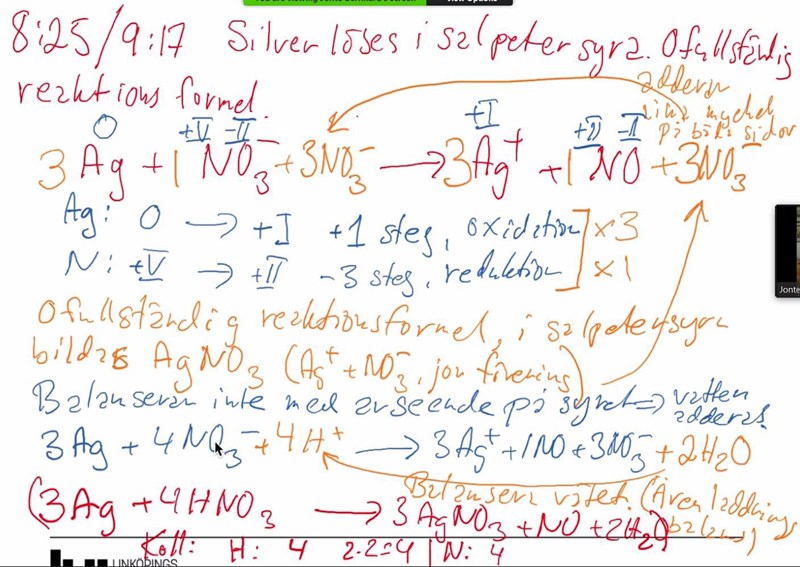
Min kemi lärare förklarade uppgiften till mig på zoom men jag förstår inte riktigt varför 3NO3^- adderas på båda sidorna av reaktionen? Måste man kunna detta utantill eller finns det något sätt att förstå varför?
Nej, det finns ingen anledning att ha med nitratjoner på båda sidor. Jag anser att det är direkt felaktigt att ha med åskådarjoner, de gör det rörigare att se vad som verkligen händer.
Jag skulle balansera så här:
Ag(s) + NO3- =/=> Ag+ + NO(g)
Ox.tal: Ag 0 => 1, +1, N V => II, -3.
3 Ag(s)+ NO3- =/=> 3 Ag+ + NO(g) syret stämmer inte, lägg till 2 vattenmolekyler på produktsidan och 4 H+ på reaktantsidan
3 Ag(s) + NO3- (aq) + 4 H+(aq) => 3 Ag+(aq) + NO(g) + 2 H2O
Koll: laddningen stämmer
Jag anser att det är fel att skriva silvernitrat som en produkt. Det finns silverjoner och nitratjoner, inte silvernitrat. Det saknas också (aq) eller (s) eller nåt annat aggregationstillstånd.
Smaragdalena skrev:Nej, det finns ingen anledning att ha med nitratjoner på båda sidor. Jag anser att det är direkt felaktigt att ha med åskådarjoner, de gör det rörigare att se vad som verkligen händer.
Jag skulle balansera så här:
Ag(s) + NO3- =/=> Ag+ + NO(g)
Ox.tal: Ag 0 => 1, +1, N V => II, -3.
3 Ag(s)+ NO3- =/=> 3 Ag+ + NO(g) syret stämmer inte, lägg till 2 vattenmolekyler på produktsidan och 4 H+ på reaktantsidan
3 Ag(s) + NO3- (aq) + 4 H+(aq) => 3 Ag+(aq) + NO(g) + 2 H2O
Koll: laddningen stämmer
Jag anser att det är fel att skriva silvernitrat som en produkt. Det finns silverjoner och nitratjoner, inte silvernitrat. Det saknas också (aq) eller (s) eller nåt annat aggregationstillstånd.
Tack så mycket nu fattar jag äntligen.


