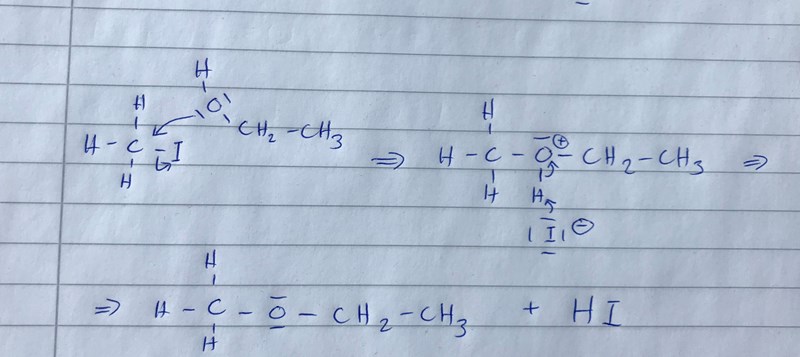SN1 och SN2
Hej, jag har lite funderingar kring dessa två varianter av substitutionsreaktioner (SN1 OCH SN2). Hur ser man vilken reaktion som är vad? Jag vet att SN1 reaktioner sker i två led och SN2 reaktioner i ett led. Hur avgör man dock hur många led reaktionen sker i? Använder man på något sätt hur balanserad karbokatjonen är för att se hur många led det är? Jag förstår dock inte riktigt hur man ser om karbokatjonen är balanserad.
Tack på förhand
Den viktigaste faktorn är ifall substituenten binder till ett primärt, sekundärt eller tertiärt kol. Det är nästan omöjligt att få till en SN2-reaktion med ett tertiärt kol eftersom elektronmolnen hos omgivande alkylgrupper blockerar och skärmar av nukleofilen. Då krävs att substituenten först lämnar (hastighetsbegränsande steget) så att nukleofilen sedan kan ges utrymme att attackera den uppstådda karbokatjonen. Ett typiskt exempel på SN1 är reaktionen mellan en hydroxidjon och 2-jod-2-metylpropan under bildning av en jodidjon och 2-metylpropan-2-ol.
I övrigt dominerar SN2-reaktioner fast i konkurrens med eliminationsreaktioner. Vilken reaktion som huvudsakligen sker går att styra i en viss riktning genom val av lösningsmedel. I många fall får man dock biprodukter då flera typer av reaktioner kan ske på samma gång. Det behövs ofta efterföljande reningssteg där man separerar just den förening man är ute efter.
Teraeagle skrev:Den viktigaste faktorn är ifall substituenten binder till ett primärt, sekundärt eller tertiärt kol. Det är nästan omöjligt att få till en SN2-reaktion med ett tertiärt kol eftersom elektronmolnen hos omgivande alkylgrupper blockerar och skärmar av nukleofilen. Då krävs att substituenten först lämnar (hastighetsbegränsande steget) så att nukleofilen sedan kan ges utrymme att attackera den uppstådda karbokatjonen. Ett typiskt exempel på SN1 är reaktionen mellan en hydroxidjon och 2-jod-2-metylpropan under bildning av en jodidjon och 2-metylpropan-2-ol.
I övrigt dominerar SN2-reaktioner fast i konkurrens med eliminationsreaktioner. Vilken reaktion som huvudsakligen sker går att styra i en viss riktning genom val av lösningsmedel. I många fall får man dock biprodukter då flera typer av reaktioner kan ske på samma gång. Det behövs ofta efterföljande reningssteg där man separerar just den förening man är ute efter.
Vad är en substituent? Är det samma som en lämnande grupp?
Tack på förhand
Precis, jag syftade på den lämnande gruppen.
Teraeagle skrev:Precis, jag syftade på den lämnande gruppen.
Tack! Hur avgör jag dock vad som är den lämnande gruppen i ett fall som detta:
I detta fall lämnar ju både joden och kvävet.
Tack på förhand
Vad är det där för reaktion? Den är inte balanserad och därmed inte komplett. Börja med att skriva en balanserad reaktionsformel så kan vi resonera utifrån den.
Teraeagle skrev:Vad är det där för reaktion? Den är inte balanserad och därmed inte komplett. Börja med att skriva en balanserad reaktionsformel sp kan vi resonera utifrån den.
Det är dock så den står på mitt uppgiftspapper med frågan "avgör om det är en SN1 eller SN2".
Tack på förhand
852sol skrev:Teraeagle skrev:Vad är det där för reaktion? Den är inte balanserad och därmed inte komplett. Börja med att skriva en balanserad reaktionsformel sp kan vi resonera utifrån den.
Det är dock så den står på mitt uppgiftspapper med frågan "avgör om det är en SN1 eller SN2".
Tack på förhand
Lägg in en bild av frågan, så blir det lättare för oss att förstå.
Smaragdalena skrev:852sol skrev:Teraeagle skrev:Vad är det där för reaktion? Den är inte balanserad och därmed inte komplett. Börja med att skriva en balanserad reaktionsformel sp kan vi resonera utifrån den.
Det är dock så den står på mitt uppgiftspapper med frågan "avgör om det är en SN1 eller SN2".
Tack på förhand
Lägg in en bild av frågan, så blir det lättare för oss att förstå.
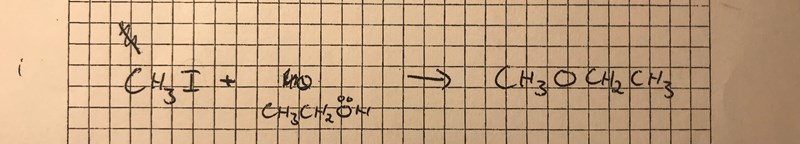
Är uppgiftslappen handskriven?
Smaragdalena skrev:Är uppgiftslappen handskriven?
Ja, av min lärare.
Då kan du säga till din lärare att hen behöver skriva så tydligt att man kan se att bokstaven längst till höger i reaktant 2 är ett H, inte ett N. (Övriga väten är nästan lika sneda!)
852sol skrev:Smaragdalena skrev:Är uppgiftslappen handskriven?
Ja, av min lärare.
Bokstaven längst till höger i reaktant 2 är ett H, inte ett N. Vilken biprodukt kan bildas av ett H och ett I?
Smaragdalena skrev:852sol skrev:Smaragdalena skrev:Är uppgiftslappen handskriven?
Ja, av min lärare.
Bokstaven längst till höger i reaktant 2 är ett H, inte ett N. Vilken biprodukt kan bildas av ett H och ett I?
HI. Men hur går det till? Lämnar kolet två elektroner till joden, men vem ger elektronpar till vem mellan syret och vätet?
Tack på förhand
Var någonstans, på vilken reaktant har du ett fritt elektronpar?
Visa spoiler
Det är t. o. m. markerat i uppgiften.
Teraeagle skrev:
Visar dock inte pilen från joden till vätet att elektronerna lämnar till vätet precis som pilen från bindningen mellan vätet och syret visar att vätet lämnar. Men är skillnaden att en pilen går från elektroner till atom vilket visar att bidning skapas och att dne andra pilen går från bindning till atom vilket visar att bindning bryts?
Hur avgör jag dock vad som är den lämnande gruppen i ett fall som detta? I detta fall lämnar ju både joden och kvävet.
Tack på förhand
Visar dock inte pilen från joden till vätet att elektronerna lämnar till vätet precis som pilen från bindningen mellan vätet och syret visar att vätet lämnar. Men är skillnaden att en pilen går från elektroner till atom vilket visar att bidning skapas och att dne andra pilen går från bindning till atom vilket visar att bindning bryts?
Syftar du på steget högst upp till höger? Den negativt laddade jodidjonen bildar en kovalent binding till vätet, som "släpper" sin kovalenta bindning till syret. Bindingselektronerna blir kvar på syret.
I detta fall lämnar ju både joden och kvävet.
Det finns fortfarande inget kväve i den här uppgiften. Jodidjonen är lämnande grupp.
Smaragdalena skrev:Visar dock inte pilen från joden till vätet att elektronerna lämnar till vätet precis som pilen från bindningen mellan vätet och syret visar att vätet lämnar. Men är skillnaden att en pilen går från elektroner till atom vilket visar att bidning skapas och att dne andra pilen går från bindning till atom vilket visar att bindning bryts?
Syftar du på steget högst upp till höger? Den negativt laddade jodidjonen bildar en kovalent binding till vätet, som "släpper" sin kovalenta bindning till syret. Bindingselektronerna blir kvar på syret.
I detta fall lämnar ju både joden och kvävet.
Det finns fortfarande inget kväve i den här uppgiften. Jodidjonen är lämnande grupp.
Skrev fel. Jag menar att vätet och joden lämnar.
Tack på förhand