Steg 3 i beta-oxidationen
Hej,
I vad jag känner till som steg 3 i beta-oxidationen lägger sig en vattenmolekyl över dubbelbindningen som skapats genom att FAD oxiderat a och b-kolen. Det jag funderar över är varför fettsyran blir en sekundär alkohol. Varför sätter sig OH-gruppen på B-kolet istället för alfa-kolet? Tänker att det inte kan ha att göra med markovnikovs regel men rätta mig gärna om jag har fel. 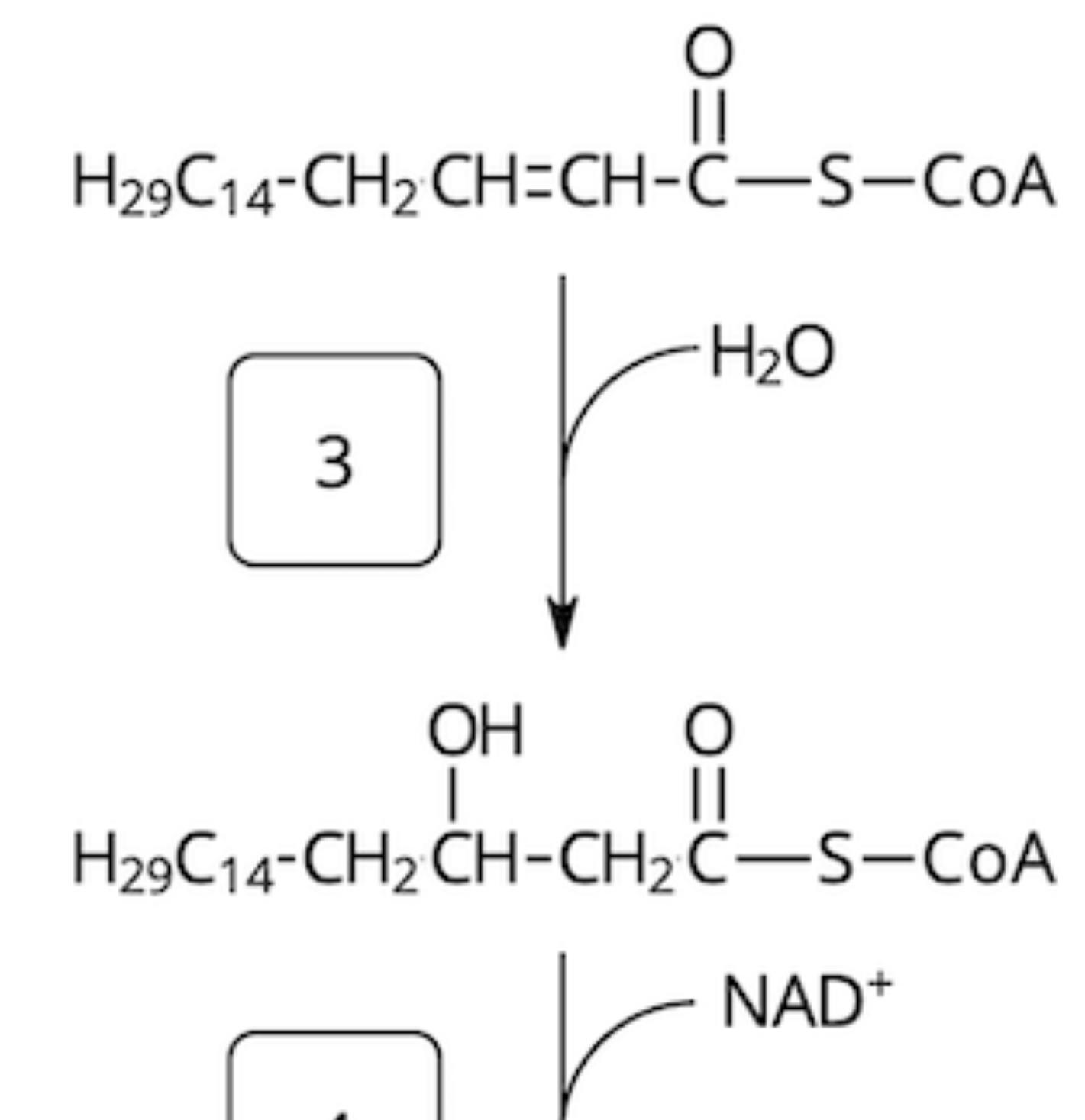
Mvh
Hej!
Det har med hur enzymer fungerar/används inom cellens biokemin, Den bygger på samma kemiska regler, men enzymerna bidrar med flera egenskaper, och dessa påverkar vilka av de termodynamiska/kemiska reglerna som bestämmer vilken reaktion som sker.
Det reaktionssteget du frågar om, utförs av ett enzym. Ett, av flera, kännetecken för enzymer är att de (oftast är) väldigt specifika för vilken reaktion som katalyseras. Det bildas med andra ord endast en eller flera bestämda produkt(er), det är m.a.o. en specifik reaktion.
För att bli specifikt har enzymet utvecklats under lång tid, till att just katalysera (ofta) endast en reaktion - en reaktionen som har behövs/behövts för cellens liv. Den biokemiska reaktionen enzymet katalyserar, är med andra ord en reaktion som behövs, och det är en reaktion som inte nödvändigtvis är den som sker enklast rent organkemiskt.
I en glaskolv i kemilabbet (eller inom processindustrin) styr kemin vilken produkt som kommer bildas, där den reaktion som sker "enklast" dominerar. Det skulle kunna ske även i cellen, och sker till viss del. Men lite av poängen med enzymer är att de katalyserar reaktioner, som normalt inte sker i cellen spontant. På så vis dessa icke-spontana reaktioner fås att ske, trots att reaktionen kräver mer aktivering (antingen i form av värme, eller genom att enzymet sänker aktiveringsenergin).
Skulle du t.ex. i en glaskolv hetta upp acyl-CoA (högst upp) med vatten till hög temperatur, skulle istället endast bindningen mellan C-S brytas, då vatten adderas och CoA-SH lämnar. Parallellt med den reaktionen, kan många andra reaktioner ske, t.ex. addering av vatten till dubbelbindningen (och denna gång domineras bildningen av produkt, av vilken reaktion som har lägst aktiveringsenergi).
De enzymkatalyserade reaktionerna i cellen, är sådan som inte sker spontant och/eller snabbt nog, vid "cellens normala förhållanden". Det är ju precis därför det behövs en biologisk katalysator i form av enzymet. Skulle det ske massvis med parallella spontana kemiska reaktioner i cellen, bildas och modifieras massvis med potentiellt oanvändbara/skadliga ämnen - vilket inte är kompatibelt med en stabil och ordnad miljö, d.v.s. det som cellen behöver för att överleva.
När reaktionerna i cellens metabolism istället är beroende av enzymer, kan ganska stabila substrat/produkter modifieras/bildas i cellen i flera steg. Ämnena kan existera i cellen och diffundera mellan ett enzym till ett annat, utan att reagera spontant med något annat ämne och brytas ner innan ämnet kommer till nytta. Samtidigt kan cellen styra vad som bildas, genom att ändra aktiviteten hos de olika enzymerna. Många av ämnena i metabolismen kan ombildas på flera olika vis till olika slutprodukter genom olika reaktioner, som var och en utförs av specifika enzymer. Så genom att ändra aktiviteten hos de olika enzymerna kan rätt mängd av rätt produkt bildas.
Det var en del om enzymer, och det korta svaret på din fråga är - att just den reaktionen sker, är för att enzymet är utvecklat för att endast katalysera den reaktionen. Vill du få en annan reaktion att ske (B), t.ex. med addition av vatten på alfa-kolet, behöver du ett annat enzym (som är utvecklat för att katalysera just den reaktionen). Men då behöver även enzymet som modifierar produkten från (B) också ändras, så att det enzymet kan modifiera ämnet med hydroxigruppen på alfa-kolet - det blir en annan reaktion i nästa modifiering av ämnet.
Enzymerna följer de (organ)kemiska reglerna, men (!) m.h.a. enzymet kan substraten placeras på lite "obekväma sätt" i förhållande till varandra, positioner som inte uppstår så lätt i t.ex. vatten. Och i de mer obekväma positionerna kommer substraten så nära varandra att de kan fås att reagera på ett sätt som inte är det lättaste i vatten (eller reaktioner som knappt är möjliga att få att ske i vatten). Det som skapas i enzymet är ett speciellt övergångstillstånd (det enda TS som ger just den specifika produkten), och detta tillstånd skapas i en miljö (enzymet) där aktiveringsenergin för denna reaktion samtidigt sänks. Resultatet blir att endast en produkt bildas (selektivitet) och att produktbildningen kan ske i t.ex. en cell vid en lägre temperatur som är möjlig för cellen att överleva (aktiveringsenergin sänks av katalysatorn).
mag1 skrev:Hej!
Det har med hur enzymer fungerar/används inom cellens biokemin, Den bygger på samma kemiska regler, men enzymerna bidrar med flera egenskaper, och dessa påverkar vilka av de termodynamiska/kemiska reglerna som bestämmer vilken reaktion som sker.
Det reaktionssteget du frågar om, utförs av ett enzym. Ett, av flera, kännetecken för enzymer är att de (oftast är) väldigt specifika för vilken reaktion som katalyseras. Det bildas med andra ord endast en eller flera bestämda produkt(er), det är m.a.o. en specifik reaktion.
För att bli specifikt har enzymet utvecklats under lång tid, till att just katalysera (ofta) endast en reaktion - en reaktionen som har behövs/behövts för cellens liv. Den biokemiska reaktionen enzymet katalyserar, är med andra ord en reaktion som behövs, och det är en reaktion som inte nödvändigtvis är den som sker enklast rent organkemiskt.
I en glaskolv i kemilabbet (eller inom processindustrin) styr kemin vilken produkt som kommer bildas, där den reaktion som sker "enklast" dominerar. Det skulle kunna ske även i cellen, och sker till viss del. Men lite av poängen med enzymer är att de katalyserar reaktioner, som normalt inte sker i cellen spontant. På så vis dessa icke-spontana reaktioner fås att ske, trots att reaktionen kräver mer aktivering (antingen i form av värme, eller genom att enzymet sänker aktiveringsenergin).
Skulle du t.ex. i en glaskolv hetta upp acyl-CoA (högst upp) med vatten till hög temperatur, skulle istället endast bindningen mellan C-S brytas, då vatten adderas och CoA-SH lämnar. Parallellt med den reaktionen, kan många andra reaktioner ske, t.ex. addering av vatten till dubbelbindningen (och denna gång domineras bildningen av produkt, av vilken reaktion som har lägst aktiveringsenergi).
De enzymkatalyserade reaktionerna i cellen, är sådan som inte sker spontant och/eller snabbt nog, vid "cellens normala förhållanden". Det är ju precis därför det behövs en biologisk katalysator i form av enzymet. Skulle det ske massvis med parallella spontana kemiska reaktioner i cellen, bildas och modifieras massvis med potentiellt oanvändbara/skadliga ämnen - vilket inte är kompatibelt med en stabil och ordnad miljö, d.v.s. det som cellen behöver för att överleva.
När reaktionerna i cellens metabolism istället är beroende av enzymer, kan ganska stabila substrat/produkter modifieras/bildas i cellen i flera steg. Ämnena kan existera i cellen och diffundera mellan ett enzym till ett annat, utan att reagera spontant med något annat ämne och brytas ner innan ämnet kommer till nytta. Samtidigt kan cellen styra vad som bildas, genom att ändra aktiviteten hos de olika enzymerna. Många av ämnena i metabolismen kan ombildas på flera olika vis till olika slutprodukter genom olika reaktioner, som var och en utförs av specifika enzymer. Så genom att ändra aktiviteten hos de olika enzymerna kan rätt mängd av rätt produkt bildas.
Det var en del om enzymer, och det korta svaret på din fråga är - att just den reaktionen sker, är för att enzymet är utvecklat för att endast katalysera den reaktionen. Vill du få en annan reaktion att ske (B), t.ex. med addition av vatten på alfa-kolet, behöver du ett annat enzym (som är utvecklat för att katalysera just den reaktionen). Men då behöver även enzymet som modifierar produkten från (B) också ändras, så att det enzymet kan modifiera ämnet med hydroxigruppen på alfa-kolet - det blir en annan reaktion i nästa modifiering av ämnet.
Enzymerna följer de (organ)kemiska reglerna, men (!) m.h.a. enzymet kan substraten placeras på lite "obekväma sätt" i förhållande till varandra, positioner som inte uppstår så lätt i t.ex. vatten. Och i de mer obekväma positionerna kommer substraten så nära varandra att de kan fås att reagera på ett sätt som inte är det lättaste i vatten (eller reaktioner som knappt är möjliga att få att ske i vatten). Det som skapas i enzymet är ett speciellt övergångstillstånd (det enda TS som ger just den specifika produkten), och detta tillstånd skapas i en miljö (enzymet) där aktiveringsenergin för denna reaktion samtidigt sänks. Resultatet blir att endast en produkt bildas (selektivitet) och att produktbildningen kan ske i t.ex. en cell vid en lägre temperatur som är möjlig för cellen att överleva (aktiveringsenergin sänks av katalysatorn).
Tack för ditt informativa och bra svar, förstår nu (:

