Sur/Basisk miljö - att lösa ut metalljoner i naturen
Bilden nedan. Man har Al(OH)2^+ som är olöslig.
1) när man säger olöslig - menar man då att den sitter fast i något i sten/jorden eller att den inte kan sönderdelas till Al-jon och OH-jon? Eller: (se fråga 2) )
2) Det står att i den streckade regionen kan Al(OH)3 bildas. Reagerar Al(OH)2^+ med OH- i en basisk miljö och bildar Al(OH)3? Är de DESSA som är det man syftar på som olösliga?
3) Men hur än svaret är på 1) och 2)
Varför blir surare miljö att Al3+ löses ut? Jag hade tänkt mig en reaktion i stil med
Al3+ + OH- <--> Al(OH)x
Om man tillsätter OH- (basisk miljö) tänker jag mer Al3+ kan bindas upp, att naturen försöker få bort överskottet av OH- som ruckar jämvikten och det kan ske genom att Al3+ reagerar till Al(OH)x.
Rätt?
4) men vad sker om inte Al3+ finns tillgängligt - blir det helt enkelt en basisk miljö då, alltså att OH- stannar som baser istället för att bindas upp?
5) Om man tillsätter H+ vet jag inte hur jag ska tänka.
Är det att de reagerar med OH- (starkast bas reagerar med starkast syra, rätt? ) och då "fattas" OH- i jämvikten så Al(OH)x löses upp. Med andra ord bildas mer Al3+ också?
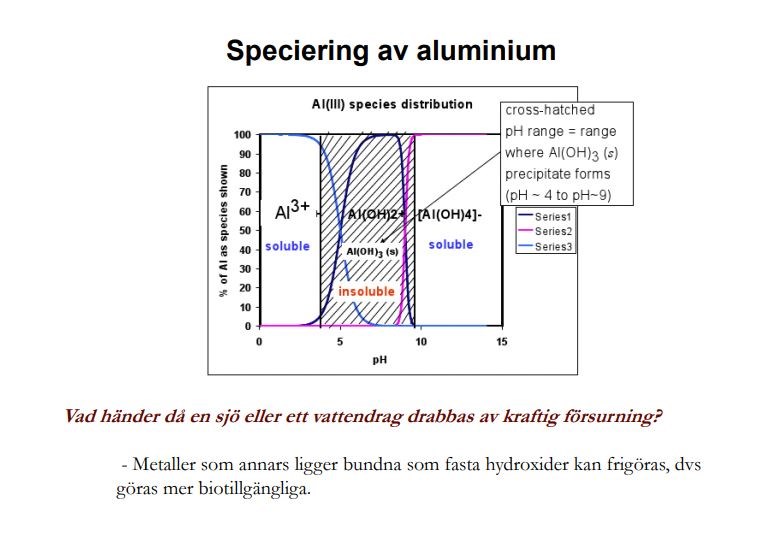
1) 2) Al(OH)2+ är i allra högsta grad vattenlöslig. Man kan inte fälla ut en ensam jon. Grafen visar att det är Al(OH)3 som är olösligt.
3) Rätt. Att göra lösningen surare är samma sak som att minska koncentrationen av hydroxidjoner. Då förskjuts jämvikten åt vänster.
4) Ja, de finns som fria hydroxidjoner i vattnet.
5) Ja, så kan man se på det.
Som sagt, du borde repetera Ke1.
Teraeagle har förklarat varför vissa metalljoner har sura egenskaper här.
Ott olösligt salt är ett salt som inte (eller rättare sagt i väldigt liten omfattning) löser upp sig till sina joner i vattenlösning.
Om pH är lågt ( d v s i sur miljö) så är aluminiumsalter lösliga. De delar uppsig till aluminiumjoner och negativa joner.
Om pH ligger mellan ungefär 4 ovch 9 så kan det bildas fällning av olösligt Al(OH)3.
Om pH är tillräckligt basiskt bildas komplexet [Al(OH)4]- eller andra komplex med ännu högre negativ laddning.
En sjö har från början ett pH som ligger strax under 7, i alla fall betydligt över pH=3. Om det tillförs sura ämnen till sjön, så kommer de i första hand att reagera med exempelvis vätekarbonatjoner som finns i vattnet. Vattnet är buffrat och pH sjunker inte så mycket som man skulle kunna tro, så länge det finns kvar av det buffrande ämnet. Hur bra buffrat vattnet är bedöms genom att mäta vattnets alkalinitet. När de buffrande ämnena har förbrukats, kommer en ytterligare tillsats av oxoniumjoner att leda till att pH sjunker. När pH går under 3, kommer aluminiuminnehållande slter (som det finns väldigt gott om i marken) att lösas upp, så att koncentrationen av aluminium i vattnet höjs betydligt.



