Syntes av lidokain, reaktions mekanism
Hej, jag kom så länge i uppgiften o har fastnat i sista delen, där det finns Ph-NH2 som ska binda till Cl-C-C-O vart ska den andra vätet ta vägen? O hur? Blir nu osäker på det jag gjort… jag följer denna texten i mitt arbete
Dimetylanilin och ättiksyra blandas
kloracetylklorid tillsättes sakta med hjälp av en pasteur pipett.
Reaktionsblandningen placeras i ett värmeblock
en 0,3 M lösning av natriumacetat i vatten tillsättes under omrörning. Blandningen kyles på ett

Kanske du kan rotera bilden så blir det mindre nackspärr för oss?
Förlåt jag fixar!!
och jag har skrivit ph-NH2 istället för dimetylanilin, jag vet att det fel och kommer att fixa det men det var enklare för mig, kommer fixa sen så klart
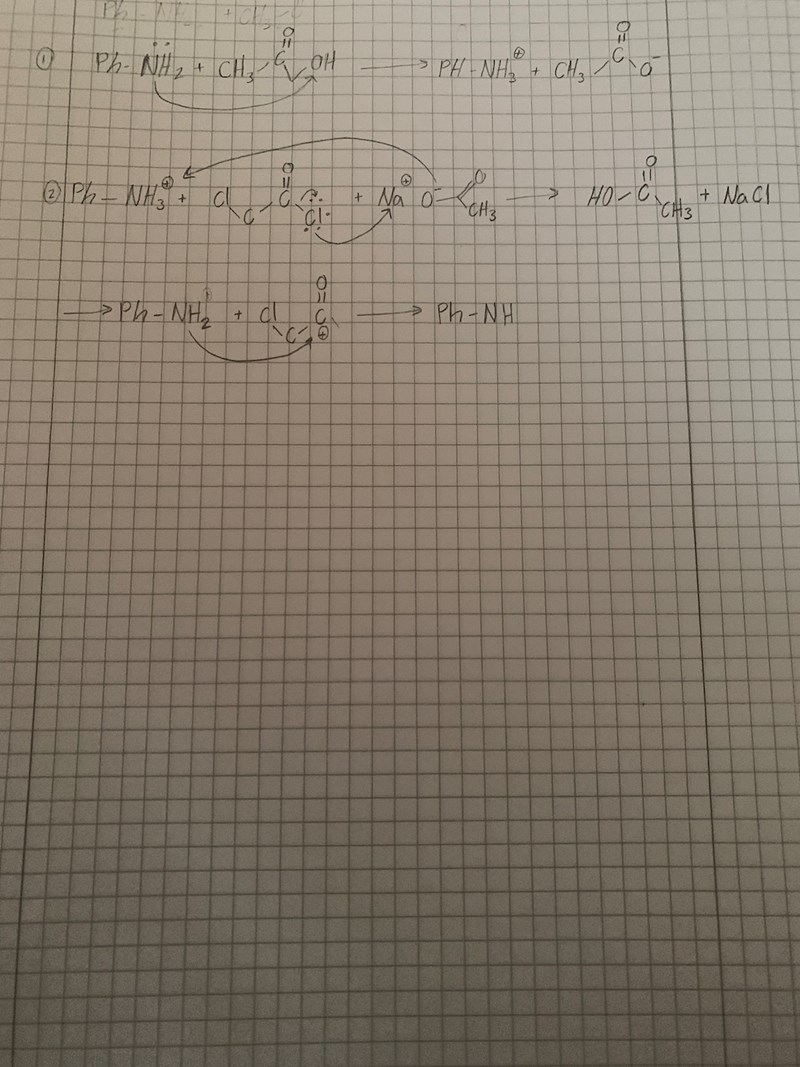
Aminogruppen i N,N-dimetylanilin (DMA) kan protoneras som du ritat i (1), men då händer inget - för när kvävets fria elektronpar har tagit upp en proton sitter det där nöjt med sin plus ett laddning. När aminogruppen har protonerats (till R-NH3+) har den fyra bindningar och kan inte skapa en bindning till kloracetylkloriden. Men lyckligtvis står denna protonerade formen i jämvikt med den oladdade, så DMA finns och kan reagera.
Gällande steg (2) i din bild. Kloridjonen kan inte lämna som du ritat, för då skapas en (superreaktiv) karbokatjon och kolatomen är redan deltapositiv (syret och kloren drar i bindingselektronerna). Den kloratomen är dock en bra lämnande grupp, men då behöver den delta positiva kolatomen skapa en annan bindning (för att släppa ifrån sig bindningselektronerna till kloratomen). Så det sker inte som du ritat i (2), men du är på rätt väg i sista raden (3).
Utgå istället ifrån att aminogruppens fria elektronpar kan agera som nukleofil, och gärna reagerar med en elektrofil kolatom...
Så om jag har fattat så är första steget rätt? Men andra är fel? Eller? Och hur menar du att jag ska fortsätta? Jag fattar inte riktigt
Det du visat på (1) är bara en syra och en bas som utbyter en proton. Men detta sker som sagt även tillbaka (denna protonövergång är reversibel). Och detta protonbytande påverkar inte direkt reaktionerna som behöver ske för att syntetisera lidokain.
För att skapa en bindning, t.ex. mellan DMA och kloracetylkloriden, så behöver några elektroner från den en reaktantens elektroner söka sig till den andra reaktanten. Och i sista raden har du ritat ut att aminogruppens fria elektronpar attackerar kloracetylkloriden, vilket är korrekt. Men det är kloracetylkloriden som attackeras på just det kolet, men detta kol är deltapositivt inte en karbokatjon. Denna reaktionen är av typen SN2 (inte SN1 som du visat, för det kan inte bildas en karbokatjon från kloracetylkloriden under de reaktionsförhållanden som du har).
Men om det är så enkelt mellan DMA och kloracetatklorid, varför har vi natriumacetat och ättiksyra? Vad gör de ens typ? O vart i det hela agerar de
Krul tepes skrev:Men om det är så enkelt mellan DMA och kloracetatklorid, varför har vi natriumacetat och ättiksyra? Vad gör de ens typ? O vart i det hela agerar de
Ja så klart behövs natriumacetatet och ättiksyran. Många reaktioner sker i en vätska, precis som denna, så det behövs ett lösningsmedel, vilket är vad ättiksyran är.
Och acetatjonen är ju ättiksyrans korresponderande bas, vilket passar ypperlig då acetatjonen kan ta upp protoner som frisätts. Om du räknar antalet protoner i aminogruppen, före (R-NH2) och efter reaktionen (R-NH-R2) så blir det en proton över för varje molekyl produkt som bildas.
Så både natriumacetat och ättiksyra är bara lösningsmedel? När man tillsätter de, ändrar de inte pH värdet? Jag vet nu vad ättiksyra gör men hur är det för natriumacetat?
Jo de påverkar pH.
Vad händer om en acetatjon tar upp en proton, vilket ämne bildas då?
Det bildas väl ättiksyra?
Precis. Varifrån tror du protonen som tas upp kommer ifrån?
Jag är mycket osäker men natriumacetat?
Nej, för en acetatjon bildas när ättiksyra protolyseras motsvarande:
CH3-COOH H20 => CH3-COO- + H3O+
Acetatjonen är en bas, som kommer att ta upp protoner.
I samband med att bindningen skapas mellan DMA och kloracetylkloriden kommer aminogruppen gå från R-NH2 till RN+H2-R, och i denna senare form har kvävet fyra bindningar (och strävar efter att ha tre) - så då kommer en av vätena protolyseras bort. Och för att ta emot detta väte finns acetatjonen.
Jaha okej, då fattar jag allt som sker, tack så mycket!
För all del, kul att det hjälpte!

