Syror och baser- jämvikt
Vilken indikator bör användas för en titreing av 0,10 M KH2BO3 och 0,10 M HCL
På facit står det att 0,05 M H3BO3 produceras vilket jag inte kan förstå. Förhållandet är väl 1:1:1?
H2BO3- + H3O+ --H3BO3 + H2O
Ja det låter som ett tryckfel.
En sådan lösning stod både på facit och en elevs lösning. Det är alltså mer än en källa som anger det som 0,05 M. Är det något jag kan ha glömt ta hänsyn till?
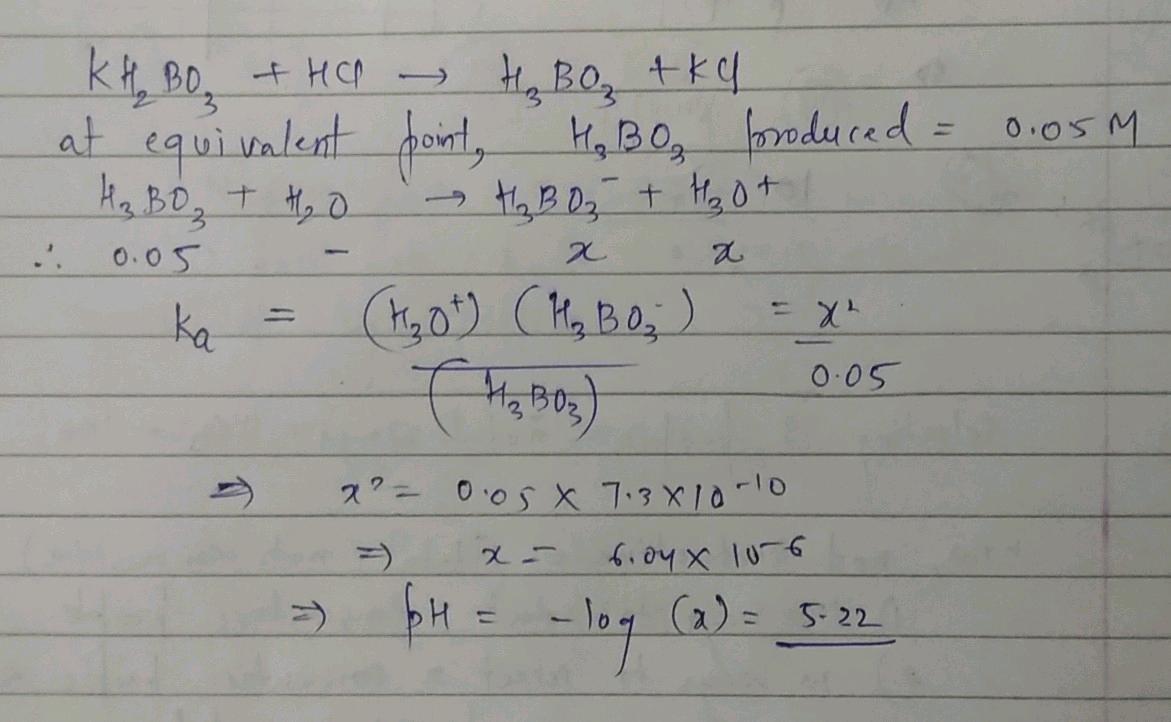
Ja okej, jag slarvläste ditt ursprungliga inlägg. Att det blir som det blir beror på att du tillsätter lika stor volym av saltsyran som provet du titrerade (ekvivalensförhållande 1:1 och de har lika hög koncentration). Hade du 100 ml prov behöver du tillsätta 100 ml saltsyra för att nå ekvivalenspunkten, vilket innebär att titrandens volym då är 200 ml. Med andra ord blir koncentrationen borsyra hälften av den ursprungliga koncentrationen kaliumdiväteborat. Volymen har fördubblats.
Men då förstår jag! :) Tack så mycket!


