Termodynamik, sluttemperatur

Hur ställer jag upp en ekvation för hur jag löser ut sluttemperaturen?
Har suttit i timmar och testat olika lösningar men får alltid fel.
Här är starten på alla mina försök. Tror det är redan här jag gör fel.
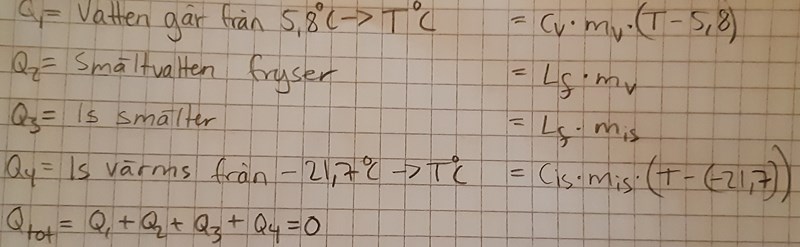
Börja med en gissning. Vad tror du händer när du häller ca 3 dl 5-gradigt vatten på 4 kg -22-gradig is? Tror du att vattnet fryser eller tror du att isen smälter?
Om du t.ex. tror att vattnet fryser så skulle jag börja med att använda dina formler för Q1 och Q2. Sen kan du kolla om Q1+Q2 räcker till att smälta isen med hjälp av Q4. Om den gör det så gissade du fel och då vet du att isen smälter. Nu vet du om sluttillståndet är flytande eller fast.
Därefter använder du de av dina ekvationer som är relevanta för ditt fall. Vid sluttillståndet har all massa samma temperatur.
Om du inte kommer hela vägen fram så är det bara att fråga igen.
Peter skrev:Börja med en gissning. Vad tror du händer när du häller ca 3 dl 5-gradigt vatten på 4 kg -22-gradig is? Tror du att vattnet fryser eller tror du att isen smälter?
Om du t.ex. tror att vattnet fryser så skulle jag börja med att använda dina formler för Q1 och Q2. Sen kan du kolla om Q1+Q2 räcker till att smälta isen med hjälp av Q4. Om den gör det så gissade du fel och då vet du att isen smälter. Nu vet du om sluttillståndet är flytande eller fast.
Därefter använder du de av dina ekvationer som är relevanta för ditt fall. Vid sluttillståndet har all massa samma temperatur.
Om du inte kommer hela vägen fram så är det bara att fråga igen.
Nu blev det fel igen. Förstår inte riktigt vad det är jag missförstår.

Det här med tecken kan vara lite lurigt. Om vi börjar med att bestämma oss för att titta på mängden energi som tillförs isen. Isen måste "ta energi" från vattnet för att kyla det till 0 grader. Sen måste isen "ta" mer energi från vattnet för att frysa det. Därför måste både Q1 och Q2 ha samma tecken. Med vår ansats att titta på mängden energi som tillförs isen så blir tecknet '+'.
Alltså för att allt vatten ska frysa så måste isen tillföras Q1 + Q2= 8,278 +112,9 kJ (jag litar på dina siffror, jag kontrollräknar inte)
Sen kollar vi om denna energi räcker för att smälta isen kJ. Det krävs 1544 kJ för att smälta isen men vattnet kan bara bidra med 113 kJ innan det fryser. Alltså fryser vattnet.
Sen får du sätta upp en ekvation för vilken sluttemperatur det blir. Vattnet har blivit 0 gradig is samtidigt som isen har blivit varmare p.g.a. de ca 113kJ som krävdes för att frysa vattnet. Men detta kan ju inte vara slutstadiet. Temperaturen måste ju bli jämn. Temperaturen för den ursprungliga isen blir Tslut samtidigt som temperaturen för den 0-gradiga isen blir Tslut. Där har du ekvationen och tempen vid slutstadiet.
Peter skrev:Det här med tecken kan vara lite lurigt. Om vi börjar med att bestämma oss för att titta på mängden energi som tillförs isen. Isen måste "ta energi" från vattnet för att kyla det till 0 grader. Sen måste isen "ta" mer energi från vattnet för att frysa det. Därför måste både Q1 och Q2 ha samma tecken. Med vår ansats att titta på mängden energi som tillförs isen så blir tecknet '+'.
Alltså för att allt vatten ska frysa så måste isen tillföras Q1 + Q2= 8,278 +112,9 kJ (jag litar på dina siffror, jag kontrollräknar inte)
Sen kollar vi om denna energi räcker för att smälta isen kJ. Det krävs 1544 kJ för att smälta isen men vattnet kan bara bidra med 113 kJ innan det fryser. Alltså fryser vattnet.
Sen får du sätta upp en ekvation för vilken sluttemperatur det blir. Vattnet har blivit 0 gradig is samtidigt som isen har blivit varmare p.g.a. de ca 113kJ som krävdes för att frysa vattnet. Men detta kan ju inte vara slutstadiet. Temperaturen måste ju bli jämn. Temperaturen för den ursprungliga isen blir Tslut samtidigt som temperaturen för den 0-gradiga isen blir Tslut. Där har du ekvationen och tempen vid slutstadiet.
Förlåt men jag förstår verkligen inte hur jag ska göra. Ska jag lägga till ett nytt Q för när vattnet går från 0°C till Tslut?
Just nu har jag försökt med:
Q5= "nyisen" går från 0°C till Tslut
Q6= isen går från -21,7°C till T slut
Q5=Q6
Och hur får jag T ensamt i en ekvation. Hur jag än gör får jag antingen T² eller T/T och alla exempel i boken har bara ett T kvar vid slutet av uträkningen.
Du är nära. Du glömmer att isen har blivit varmare när den frös vattnet till is, så den går inte från -21,7. Vi tar det stegvis precis som du har gjort:
- Isen kyler vattnet till 0 grader
Dessa 7,25 kJ har alltså lämnat vattnet och upptagits av isen som då blir varmare eftersom den har upptagit energi.
- Isen fryser det nollgradiga vattnet (här använder jag Lf=333 kJ/kg)
Nu har isen tagit upp ca 120 kJ.
- Hur mycket varmare har isen blivit nu?
Här kan du sätta in värden och räkna ut T1. Nu har vi is med temperatur T1 och lite mindre is med temperatur 0. Den varma isen kommer att avge energi. Samma mängd energi kommer den kalla isen att ta upp. Till slut får allt samma temperatur Tslut. Sen sätter vi upp ekvationen som säger just detta:
- Den avgivna mängden energi är samma som den upptagna:
Det syns kanske inte så tydligt men det är bara Tslut som är okänd här och det är en "vanlig" förstagradsekvation. Inga kvadrater eller så. Sätt in värden, multiplicera in faktorerna framför parenteserna och samla alla Tslut på samma sida. Precis som vanligt. Jag får Tslut till ca. -6,8. Du behöver vara noggrannare än mig med värdesiffror.
Men, det här med tecken då? Hur vet man vilken ordning man ska ha när man beräknar temperaturdifferenserna? Det ser ju helt slumpmässigt ut ovan!
Visa spoiler
Jag måste erkänna att jag blev lite yr av temperaturdifferenserna. Ett sätt att tänka är att bara räkna med positiva energier precis som jag har gjort ovan. Sen får man tänka till om vad som händer, vem avger energi och vem upptar energi. Om energin alltid ska vara positiv så måste man se till att parentesen med differensen är positiv (m och c är ju alltid positiva). Då blir hela produkten positiv. Om differensen ska vara positiv så ska alltid den högsta temperaturen stå först. Jämför sista ekvationen. Tslut är högre än T1 (den ursprungliga isen blir varmare) och 0 är högre än T1 (det ursprungliga vattnet blir kallare).

