termokemi
Vad är skillnad mellan H och Hf ? Finns det någon uppgift där man behöver använda båda?
Feswa skrev:Vad är skillnad mellan H och Hf ? Finns det någon uppgift där man behöver använda båda?
∆H är entalpiskillnaden för en reaktion.
∆Hf för en kemisk förening är entalpiändringen när 1 mol av ämnet framställs från grundämnena. Det är mycket lättare att göra en tabell för ∆Hf eftersom man är överens om var noll-nivå ligger.
Ja, man kan behöva båda i samma uppgift.
Finns det något exempel en en sådan uppgift som kräver båda?
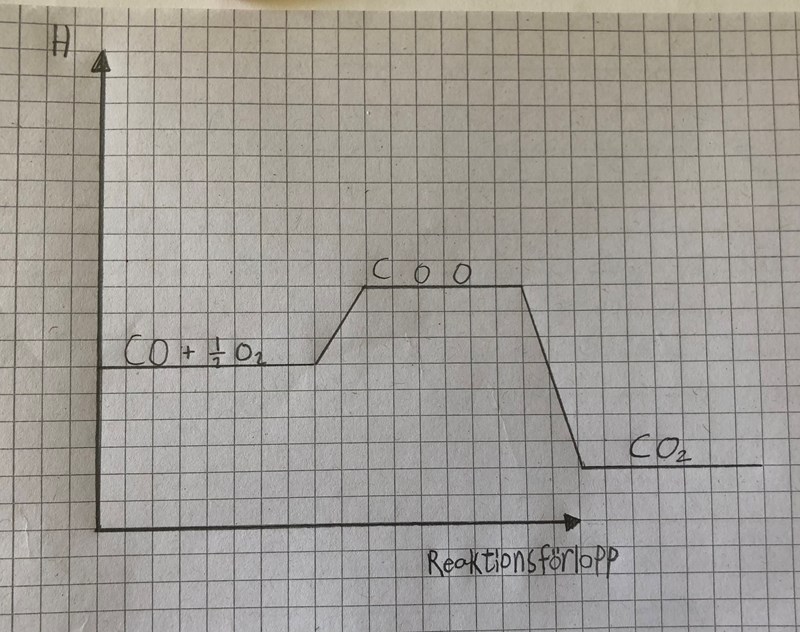
Är reaktionen CO + ½ O2 => CO2 exoterm eller endoterm?
Hur löser man den uppgiften?
Börja med att slå upp ∆Hf för CO och CO2. Sedan skulle jag rita ett energinivådiagram, för jag tycker det är så lätt att göra teckenfel annars.
exoterm?
Korrekt, men det intressanta är inte svaret, utan vägen dit.
hur beräknar man det?
Feswa skrev:
hur beräknar man det?
Det beskrev jag här:
Smaragdalena skrev:Börja med att slå upp ∆Hf för CO och CO2. Sedan skulle jag rita ett energinivådiagram, för jag tycker det är så lätt att göra teckenfel annars.
∆Hf CO är -110 kJ/mol och ∆Hf CO2 är -394 kJ/mol
Lägg upp ditt diagram här.
varför har O2 inget ∆Hf?
Feswa skrev:varför har O2 inget ∆Hf?
Vad menar du med att ∆Hf inte har något värde? ∆Hf = 0, helt i enlighet med definitionen av ∆Hf.
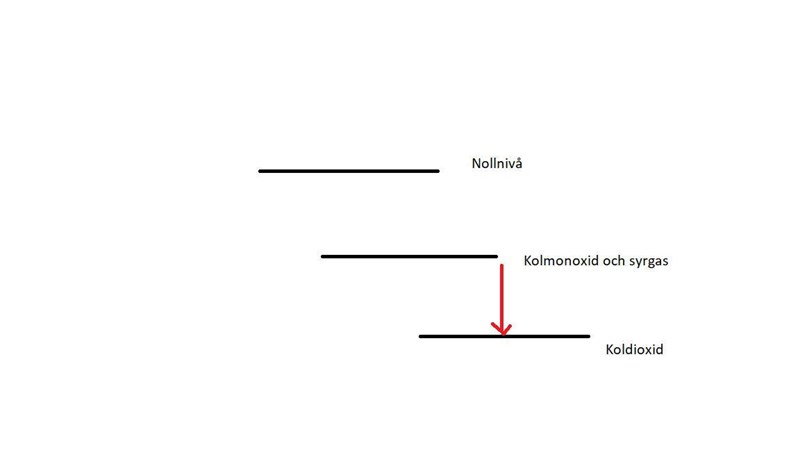
Den röda pilen är .