termokemi bindningsentalpi
Hej!
Jag har fastnat på en ytterligare fråga:
Kolmonoxid har bildningsentalpin ∆H = -110 kJ/mol.
Koldioxid har bildningsentalpin ∆H = -394 kJ/mol.
Ange entalpiändringen då 1 mol kolmonoxid förbränns till koldioxid i syrgas.
Varför subtraherar man på följande fråga, borde man inte addera bildningsentalpierna istället?
Tacksam för hjälp!
Du jämför två olika bindningar och vill få skillnaden mellan dem, så nej du kan inte addera dem - då får du hur mycket de är tillsammans. Istället vill du få skillnaden mellan dem så du behöver subtrahera.
hur vet man att de jämför skillnaden mellan dem?
Jag tycker termokemi är jättekrångligt om jag inte får rita upp ett diagram. Så här:
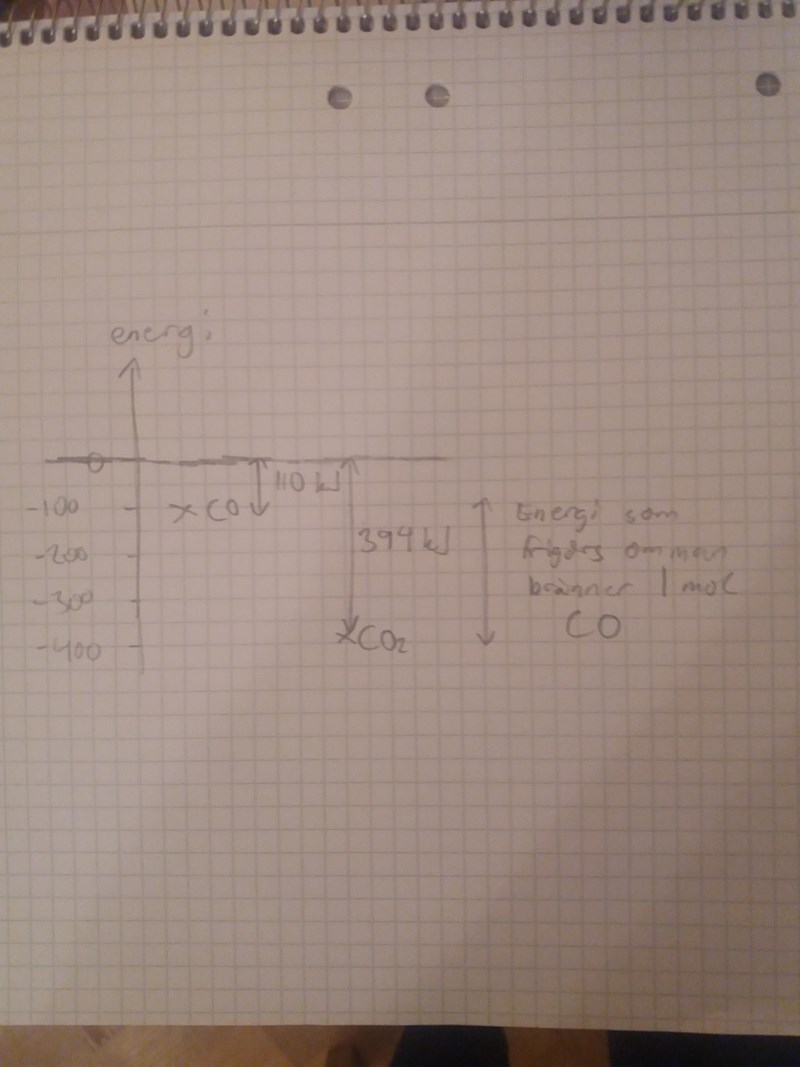
smart, och då blir entalpiändringen 264KJ?
Ja ,det frigörs 264 kJ.


