Titrering av ättiksyra i vinäger med natriumhydroxid
Hej!
Jag har genomfört en laboration där jag titrerat ättiksyra i vinäger med en natriumhydroxid och skulle sedan räkna ut masshalten ättiksyra genom att skapa en titrerkurva och använda matematiska beräkningar. Jag fick fram 5,99 % varav masshalten ska vara 6 %. I min diskussion har jag sedan skrivit att möjliga felkällor kan vara noggrannheten av volymen NaOH som droppades ner och att det dessutom kunde ha använts gamla kemikalier (vinägern) som kan ha dunstat bort vatten och bidragit till att lösningen inte innehöll den angivna koncentrationen. Min lärare har bett mig utveckla detta och skriva om hur resultatet kan påverkas av de ovanstående faktorerna och ställer frågorna: Om något har dunstat bort i vinägern, hur borde det ha påverkat halten ättiksyra? Hur ser jag om avläsning av byretten som användes blir fel? Visar titrerkurvan några avvikelser?
Jag vet inte riktigt hur jag ska utveckla mitt svar och svara på de frågor som min lärare ställer. Vore väldigt tacksam om någon kunde hjälpa mig!
Vad är det du tror kan ha avdunstat från vinägern, är det vatten, ättiksyra eller något annat? Hur påverkas halten vinäger i de olika fallen, blir den högre eller lägre?
Hur gjorde du när du läste av byretten?
Hur ser titrerkurvan ut?
Vad jag skrev att jag trodde avdunstade från vinägern var vatten. Frågan som jag ställde mig själv var då om det kunde bidra till att lösningen (vinägern) inte innehöll den angivna koncentrationen. Hur halten vinäger påverkas i de olika fallen förstår jag inte helt.
Natriumhydroxidlösningen tillsattes i portioner om 0,5-1,0 cm3 och det var så jag läste av den, direkt från byretten.
Såhär ser titrerkurvan ut: 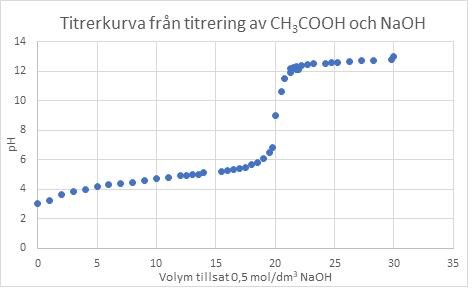
När något avdunstar, så minskar volymen. Hur påverkas koncentrationen av ättiksyra om en del av vattnet avdunstar?
Skulle ni beräkna pKa för ättiksyra också?
Koncentrationen borde väl öka då, väldigt lite. Nej vi skulle inte beräkna pKa för ättiksyra
Tack Smaragdalena för ditt svar!
Angående frågorna: Hur ser jag om avläsning av byretten som användes blir fel? Visar titrerkurvan några avvikelser?
Hur kan jag tänka där?
När man läser av en byrett skall man läsa av i botten av menisken. Den här bilden visar 20 ml, inte 19,9 eller 19,8 ml.

Aha okej, tack! Men om man har avläst fel, hur kan det ses i titrerturvan? Gör det det överhuvudtaget?
delama skrev:Aha okej, tack! Men om man har avläst fel, hur kan det ses i titrerturvan? Gör det det överhuvudtaget?
Det kan du inte se, det är en felkälla. Det är därför man ofta använder elektroder för att mäta pH i verkligheten, för att undvika den felkällan.
Hmm, okej. Tack så mycket!
Hur tänker du kring hur koncentrationen av ättiksyra påverkas som en del av vattnet avdunstar i vinägern?
Hej!
Förstår fortfarande inte om jag kan se i titrerkurvan, som avvikelse, ifall jag har läst av byretten fel.
Gällande frågan om vatten avdunstar från vinägern kan påverka koncentrationen ättiksyra, svarade jag att koncentrationen borde öka. Tänkte formeln c=n/V. Minskar volymen, ökar koncentrationen. Tänker jag rätt? Någon som vet eller kan resonera sig fram till det korrekta svaret?
Du kan inte se det i titreringskurvan men koncentrationsbestämningen blir inte helt exakt om man inte utläser rätt volym. Det är alltså din koncentration som isåfall inte skulle vara exakt den du har räknat ut. Om du tror att du titrerat för lite mot vad som är sant så kommer din koncentrationsbestämning av syran bli högre än vad den är.
Sen så blir det dubbla felkällor om koncentrationen skulle vara som du säger, högre, i och med att vatten avdunstat enligt ditt matematiska samband .
Lite off topic, men kanske intressant ändå, på tal om felkällor vid titreringar:
Natriumhydroxidlösningar har en tendens att absorbera koldioxid från luften, så att det bildas kolsyra som neutraliserar en del av natriumhydroxiden:
.
Så beroende på när och hur natriumhydroxidlösningen bereddes, så finns det en risk att den verkliga koncentrationen natriumhydroxid var lägre än den angivna. Fundera gärna på hur detta skulle detta påverka resultatet om det skedde!




