Titrering av svaga syror
Jag skulle behöva hjälp med att bestämma koncentrationen för propansyra. Det jag har gjort är att jag har titrerat 40 ml propansyra med 0,100 M NaOH tills pH:t närmat sig 13. Har gjort en tabell med pH:t innan/efter varje tillsats av 1 ml NaOH. Men jag vet inte hur jag nu ska fortsätta. Jag antar att det har med ekvivalenspunkten att göra men jag vet inte vad jag ska göra eller börja.
Jag kan se att EP är någonstans mellan 7,2 och 9,85 men hur får jag ett exakt värde?
Hur beräknar jag ekvivalenspunkten och halvtitreringspunkten?
Lägg upp en bild av titrerkurvan, så syns det förhoppningsvis var ekvivalenspunkten är.
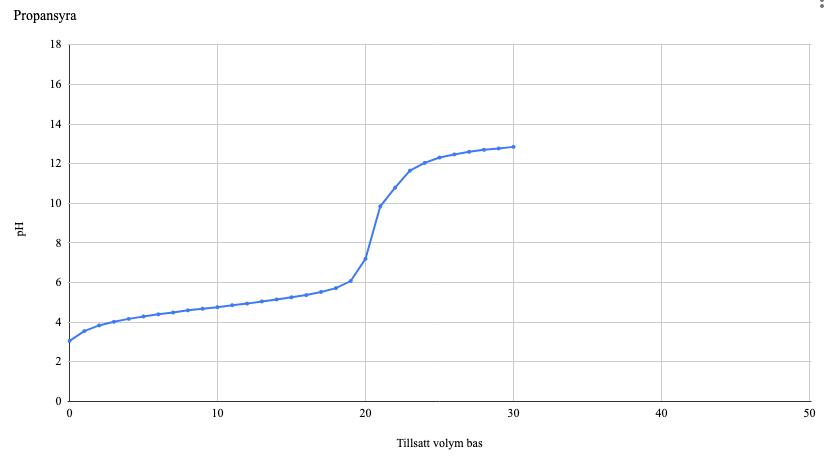
Har nu räknat det som att EP är vid pH = 9.85, när 21 ml NaOH tillsatts.
n(NaOH) = 0,100 * 0,021 = 0,0021 mol.
c(HA) = n/v = 0,0021/0,04 = 0,0525 mol/dm3.
Eller ska jag räkna det som mittemellan punkterna pH7,2 och 9,85? Alltså när V(NaOH) = 20,5?
Jag läser av kurvan som att EP ligger mellan 20 och 21 ml. Man borde ha gjort betydligt mindre tillsatser åtminstone från 20 ml så att man fick tätare värden och därmed en säkrare EP.
Halvtitrerpunkten ligger alltså vid 10,25 ml. Vilket är pH där? Detta är pKa för syran.


