Trommers prov
Om man gör Trommers prov med kopparsulfat och natriumhydroxid, är det natriumhydroxid som avger syre till sockerarten? Men det är ändå kopparsulfatet som tar upp elektronerna från sockerarten? Jag förstår liksom inte vad det har för betydelse att natriumhydroxid avger syre om det ändå inte är det ämnet som är reducerande. Man brukar väl säga att oxidation av organiska ämnen är reaktion med syre. Betyder det inte att syret är det reducerande ämnet?
Det är kopparjonen som tar upp en elektron. Syrgas är inte inblandat i den här reaktionen.
Från början betydde oxidation "reaktion med syre/syrgas". Numera har betydelsen vidgats, så att det heter oxidation även om oxidationsmedlet är något annat än syrgas.
Syre är praktiskt taget aldrig ett reducerande ämne, tvärtom! Syre reduceras, d v s syre är ett oxidationsmedel.
Smaragdalena skrev:Det är kopparjonen som tar upp en elektron. Syrgas är inte inblandat i den här reaktionen.
Från början betydde oxidation "reaktion med syre/syrgas". Numera har betydelsen vidgats, så att det heter oxidation även om oxidationsmedlet är något annat än syrgas.
Syre är praktiskt taget aldrig ett reducerande ämne, tvärtom! Syre reduceras, d v s syre är ett oxidationsmedel.
Men så att syret från natriumhydroxid binds till aldehydgruppen och bildar en karboxylgrupp har egentligen inget med själva oxidationen att göra? Eller var kommer syret ifrån? Och varför binds syret? Jag förstår liksom inte hur detta hänger ihop med redox-reaktionen, att syre binder in när det avges elektroner. Man säger ju att sockerarten oxideras till en karboxylsyra, så är det processen när den tar upp syre som är oxiderande?
Från vad du skrev sund20, verkar du ha tillsatt saltet kopparsulfat till en vattenlösning innehållande (saltet) natriumhydroxid. När de lösta jonerna stöter på varandra kommer de att möblera om lite, Na+ och SO42- kommer vara åskådarjoner så de kan du strunta i.
Cu2+ kommer att binda till sig 4 OH-, och det är i denna form som kopparjonen kommer reduceras av sockerartens aldehydgrupp.
En av dessa hydroxidjoner (bundna av kopparjonen) kommer att adderas till aldehydens kolatom, och tillsammans kommer de bilda karboxylsyran. Precis hur denna redoxreaktion sker är utanför Ke2, det är snarare universitetsnivå. (Och för att beskriva precis varför och hur detta syre adderas, behöver du kunna bestämma oxidationstalen före och efter under reaktionen i bilden nedan, där det ingår flera joner och elektronöverföringar på samma gång).
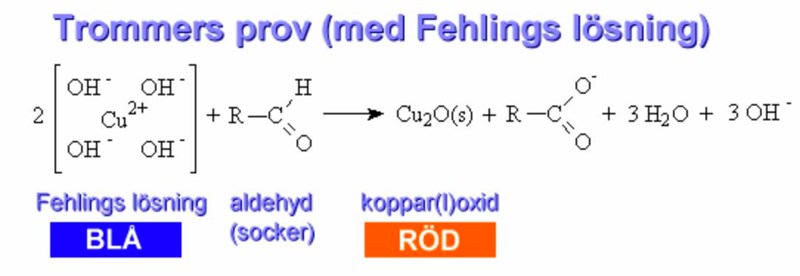
Man säger ju att sockerarten oxideras till en karboxylsyra, så är det processen när den tar upp syre som är oxiderande?
Nej inte direkt, men additionen av hydroxigruppen är en del av oxidationsdelen av redoxreaktionen. Kopparjoner reduceras även samtidigt.
mag1 skrev:Från vad du skrev sund20, verkar du ha tillsatt saltet kopparsulfat till en vattenlösning innehållande (saltet) natriumhydroxid. När de lösta jonerna stöter på varandra kommer de att möblera om lite, Na+ och SO42- kommer vara åskådarjoner så de kan du strunta i.
Cu2+ kommer att binda till sig 4 OH-, och det är i denna form som kopparjonen kommer reduceras av sockerartens aldehydgrupp.
En av dessa hydroxidjoner (bundna av kopparjonen) kommer att adderas till aldehydens kolatom, och tillsammans kommer de bilda karboxylsyran. Precis hur denna redoxreaktion sker är utanför Ke2, det är snarare universitetsnivå. (Och för att beskriva precis varför och hur detta syre adderas, behöver du kunna bestämma oxidationstalen före och efter under reaktionen i bilden nedan, där det ingår flera joner och elektronöverföringar på samma gång).
Man säger ju att sockerarten oxideras till en karboxylsyra, så är det processen när den tar upp syre som är oxiderande?
Nej inte direkt, men additionen av hydroxigruppen är en del av oxidationsdelen av redoxreaktionen. Kopparjoner reduceras även samtidigt.
Är det hela hydroxigruppen som går till sockerarten? För där sitter ju redan ett H och om det då kommer en OH-grupp så bildas väl vatten? Jag antar att anledningen till varför det bara ett O kvar i produkten är för att den protolyseras i en basisk vätska, men är det 2 H som gör det (om det nu är så att både O och H går till aldehyden)?
Är det hela aldehydgruppen som avger elektroner till kopparn? Varför blir inte molekylen positivt laddad när den avger elektoner?
Nej efter reaktionen sitter inte hela hydroxigruppen på kolhydraten, utan endast ett syre som kommer ifrån hydroxigruppen.
Ja, vätet i aldehyden lämnar som ett vatten. Det är nio H hos reaktanterna, och nio H i form av H2O och OH- i produkterna.
Ja den bildade karboxylsyragruppen protolyseras i den basiska lösningen.
Nej, hela aldehydgruppen lämnar inte ifrån sig elektroner. Hur detta sker ser du med hjälp av oxidationstalen. Alternativt kan du titta på bindningarna för att få en överblick över vad som sker. Där:
1) aldehydens väte med bindning försvinner i form av en H+, och bindningen (C-H) ger de 2 elektroner som går åt för att reducera de två kopparjonerna.
2) Detta vätet ersätts av en hydroxigrupp, där ingen förändring sker i antalet elektroner kring detta syre. Det är 8 innan (varav två delade med hydroxigruppsvätet) - och 8 efter, varav 2 delade med kolet som en del i karboxylgruppen.
3) Karboxylsyran protolyseras och bindningen mellan O-H tillfaller syret.


