Typiska farten för en molekyl i luft vid rumstemperatur?
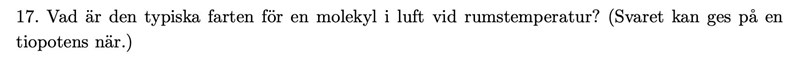
Vet att formeln k*T= E finns, och sen är det bara att använda formeln för rörelseenergi mv^2/2 antar jag. Problemet är att jag inte vet hur många atomer. Vet att 79% är kväve och 21% syre. Någon som vet mängden av alla atomer? För annars är det svår att räkna ut massan.
I detta fall tror jag att dem vill att man ska skriva att massan = 32u = (32*1.67*10^-27)kg dvs en syremolekyl. Sen är det bara att använda
1.5KT = mv^2 / 2
RandomUsername skrev:I detta fall tror jag att dem vill att man ska skriva att massan = 32u = (32*1.67*10^-27)kg dvs en syremolekyl. Sen är det bara att använda
1.5KT = mv^2 / 2
Ahh juste för syremolekylen har masstal 32u. Varför 1.5KT=mv^2/2? Vad får du koefficienten 1.5 ifrån?
formeln är 1.5KT = mv^2 / 2
Dualitetsförhållandet skrev:
Vad får du koefficienten 1.5 ifrån?
Det är ½kT i kinetisk energi i alla tre translationsriktningar.
Jag ser att din fysikkurs börjar komma in lite på statistik mekanik grejer, trevligt! (Men linjär algebra och kvantmekanik är mycket roligare am i right?).
RandomUsername skrev:formeln är 1.5KT = mv^2 / 2
Vad bör jag googla för att få fram den formeln?
Jag läser fysik 2 just nu och har den i min formelsamling men testa Kinetisk gasteori



