Uppgift i biokemi
Tja!
Har fastnat på denna uppgift: vet inte riktigt hur man ska resonera sig fram. Jag vet att rätt svar ska vara pH= 6. För att sidokedjor ska binda sig med en jonbindning behöver det finnas en negativ samt en postitiv sidokedja, längre än så har jag inte kommit 😅 .
Det finns två amingrupper och två karboxylgrupper: karboxylgruppen är lite mer sur än vad amingruppen är basisk. Detta ger oss pH= 6, däremot vet jag inte om detta har med frågan att göra.
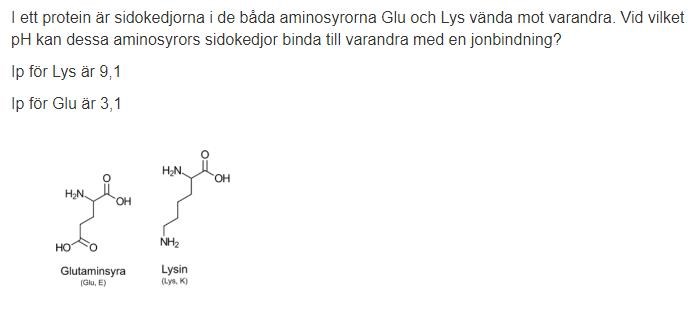
Det som avgör om dessa aminosyror kan bilda en jonbindning är deras laddning.
Samtidigt avgörs inte pH av dessa två aminosyrors sidokedjor, som i din uppgift är en del av ett protein med många fler aminosyrarester. Utan pH avgörs av den omgivande lösningens pH.
Men frågan är inte om vilket pH det är - utan istället: Vid vilket pH kan aminosyrornas sidokedjor bilda en jonbindning?
Du har sidokedjornas isoelektriska punkt, och då resonera utifrån dessa IP värden.
mag1 skrev:Det som avgör om dessa aminosyror kan bilda en jonbindning är deras laddning.
Samtidigt avgörs inte pH av dessa två aminosyrors sidokedjor, som i din uppgift är en del av ett protein med många fler aminosyrarester. Utan pH avgörs av den omgivande lösningens pH.
Men frågan är inte om vilket pH det är - utan istället: Vid vilket pH kan aminosyrornas sidokedjor bilda en jonbindning?
Du har sidokedjornas isoelektriska punkt, och då resonera utifrån dessa IP värden.
Tack för ditt svar.
Min lärare (som svarar en gång varje fullmåne) skrev precis som du, att jag nämligen ska resonera utifrån sidokedjornas IP, däremot förstår jag inte riktigt hur jag ska gå tillväga.
Min mattehjärna säger 3.1+9.1/2 = 6.. något som förmodligen är helt fel
Skulle du snälla kunna förklara ytterligare?
Tack på förhand
IP är inte samma sak som pH (du kan kolla i boken/wiki om du inte minns vad IP är).
Skulle du blanda en av varje aminosyra kanske din liknelse med att addera dem till varandra skulle likna det som sker, men pH skulle inte riktigt bli 6.
Nu har du istället ett protein som båda aminosyrorna är en del av. Och deras sidokedjor är de som kan protolyseras eller ta upp en proton - vilket är den effekt som krävs för att de skall få varsin laddning - av olika slag (+/-). När de har fått dessa motsatta laddningar kan de bilda en jonbindning.
Så om du tittar på aminosyrornas vardera IP (då ingen laddning finns), vad krävs för att de skall få en laddning?
Vid vilket pH tror du att de kommer få varsin men motsatt laddning?
mag1 skrev:IP är inte samma sak som pH (du kan kolla i boken/wiki om du inte minns vad IP är).
Skulle du blanda en av varje aminosyra kanske din liknelse med att addera dem till varandra skulle likna det som sker, men pH skulle inte riktigt bli 6.
Nu har du istället ett protein som båda aminosyrorna är en del av. Och deras sidokedjor är de som kan protolyseras eller ta upp en proton - vilket är den effekt som krävs för att de skall få varsin laddning - av olika slag (+/-). När de har fått dessa motsatta laddningar kan de bilda en jonbindning.
Så om du tittar på aminosyrornas vardera IP (då ingen laddning finns), vad krävs för att de skall få en laddning?
Vid vilket pH tror du att de kommer få varsin men motsatt laddning?
Lysin är en bas på grund av amingruppen på sidokedjan (NH2) och för att den ska få en laddning måste den ta upp en proton. Glu som är en syra kommer ge bort en proton. Lysin blir (+) och Glu blir (-)
Hur vet jag vid vilket pH detta sker?
Du vet att vid IP, saknas laddning.
För att t.ex. karboxylsyragruppen på Glu skall släppa ifrån sin proton, skall pH vara högre eller lägre än IP?
mag1 skrev:Du vet att vid IP, saknas laddning.
För att t.ex. karboxylsyragruppen på Glu skall släppa ifrån sin proton, skall pH vara högre eller lägre än IP?
Lägre tror jag
Glutaminsyrans funktionella grupp är karboxylsyran. Hur ser den ut när den saknar laddning (vid IP)?
Om du vill att den skall få laddning vad behöver då ske?
Sker detta lättare om pH sjunker (H+ koncentrationen blir större) eller när pH ökar (H+ koncentrationen minskar)?

