Varför är ättiksyra starkare än propansyra?
Hej!
Jag undrar varför ättiksyra (HAc) är starkare syra än propansyra? Jag vet att Ka-värdet för HAc är högre än propansyras Ka-värde och påvisar därför att HAc protolyseras i högre grad.
FRÅGA: Men om man kollar på deras strukturformler - vad är det i strukturen som gör att HAc har enklare för att avge en vätejon från sin hydroxylgrupp än propansyran?
Mina tankar snöar in sig på fördelningen av elektronöverskott och kokpunkter. Propansyran har fler kolatomer som kan dela på elektronöverskottet vilket gör den en aning stabilare än HAc som bara har två kolatomer. Eftersom propansyran är stabilare får den en högre kokpunkt.
MEN där tar det stopp för mig. Vad är det i syrornas strukturformler som gör att HAc enklare avger en vätejon än propansyran?
Tack på förhand!
Strukturformel ättiksyra:
.jpg?width=800&upscale=false)
Strukturformel propansyra: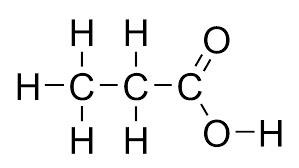
Nja, du är på rätt väg, en anledningen till varför propansyra är en starkare syra har med resonanstruktur att göra, tror du kommer läsa mer om det här i organiska kemin. När vätejonen disassocierar från syret, elektronerna tas inte med och är fortfarande kvar på syret, då syret är mer elektronegativt. Detta leder till att den laddning som uppstår behövs fördelas på något sätt, alltså resonansstruktur. Detta innebär att elektronerna kan "hoppa" mellan bidningarna och på så sätt skapar en stabilare anjon (bas). Propansyra har flera punkter där elektronerna kan fördelas (på grund av antalet kol). Därför har propansyra en starkare syra än ättika syra. Anjonen är alltså stabilare, det är lättare för vätet att lossna.
Ättiksyra är en starkare syra än propionsyra, inte tvärtom.
Det finns ett namn för detta: induktiv effekt.
lägg till myrsyra som exempel så har du en fin serie.
Olaf-Johansson skrev:Nja, du är på rätt väg, en anledningen till varför propansyra är en starkare syra har med resonanstruktur att göra, tror du kommer läsa mer om det här i organiska kemin. När vätejonen disassocierar från syret, elektronerna tas inte med och är fortfarande kvar på syret, då syret är mer elektronegativt. Detta leder till att den laddning som uppstår behövs fördelas på något sätt, alltså resonansstruktur. Detta innebär att elektronerna kan "hoppa" mellan bidningarna och på så sätt skapar en stabilare anjon (bas). Propansyra har flera punkter där elektronerna kan fördelas (på grund av antalet kol). Därför har propansyra en starkare syra än ättika syra. Anjonen är alltså stabilare, det är lättare för vätet att lossna.
Kemiboken tar upp resonans men förklarar bara att det är pga. resonans som karboxylsyror är benägna att protolyseras som syror till skillnad från alkoholer som endast har en enda syremolekyl med all negativ laddning om den skulle protolyseras som en syra.
Teraeagle skrev:Det finns ett namn för detta: induktiv effekt.
Okej, tack! Har jag förstått det rätt? Om man förklarar riktigt förenklat, är det då så att HAc är starkare syra eftersom den är mer instabil än propansyran? HAc har bara två kolatomer som kan dela på syremolekylernas elektronöverskott, medan propansyran har tre kolatomer vilket gör den mer stabil och lite motvilligare till att avge en vätejon?
Nja. Det är lite som en dragkamp i molekylen mellan syrena i karboxylgruppen och det som sitter på det andra kolet. Syreatomerna är elektronegativa och drar åt sig elektroner från resten av molekylen. Om det är hög elektrondensitet runt syret i OH-gruppen kan man nästan tänka att det ”limmar fast” H+ så att det inte kan avges lika lätt.
Om man placerar något annat elektronegativt som kloratomer i andra änden av molekylen kommer de att ha ”dragkamp” med syrena och göra så att det blir mindre sannolikt att påträffa elektronerna kring syrena. Då blir det lättare att avge H+. Triklorättiksyra är t.ex. en betydligt starkare syra än ättiksyra.
Placerar man något med lägre elektronegativitet i molekylen istället, t.ex. kol och väten i form av alkylgrupper, så blir effekten motsatt. Syrena får då fler atomer varifrån de kan attrahera ytterligare elektroner och göra OH-bindningen ännu starkare. Det är därför syrastyrkan sjunker ju längre kolkedjan blir. Riktigt långa syror som stearinsyra (18 kolatomer) är väldigt svaga medan myrsyra med sin enda kolatom är förhållandevis stark.
Teraeagle skrev:Nja. Det är lite som en dragkamp i molekylen mellan syrena i karboxylgruppen och det som sitter på det andra kolet. Syreatomerna är elektronegativa och drar åt sig elektroner från resten av molekylen. Om det är hög elektrondensitet runt syret i OH-gruppen kan man nästan tänka att det ”limmar fast” H+ så att det inte kan avges lika lätt.
Om man placerar något annat elektronegativt som kloratomer i andra änden av molekylen kommer de att ha ”dragkamp” med syrena och göra så att det blir mindre sannolikt att påträffa elektronerna kring syrena. Då blir det lättare att avge H+. Triklorättiksyra är t.ex. en betydligt starkare syra än ättiksyra.
Placerar man något med lägre elektronegativitet i molekylen istället, t.ex. kol och väten i form av alkylgrupper, så blir effekten motsatt. Syrena får då fler atomer varifrån de kan attrahera ytterligare elektroner och göra OH-bindningen ännu starkare. Det är därför syrastyrkan sjunker ju längre kolkedjan blir. Riktigt långa syror som stearinsyra (18 kolatomer) är väldigt svaga medan myrsyra med sin enda kolatom är förhållandevis stark.
Wow tack så hemskt mycket för din tid och förklaring, nu har jag det!