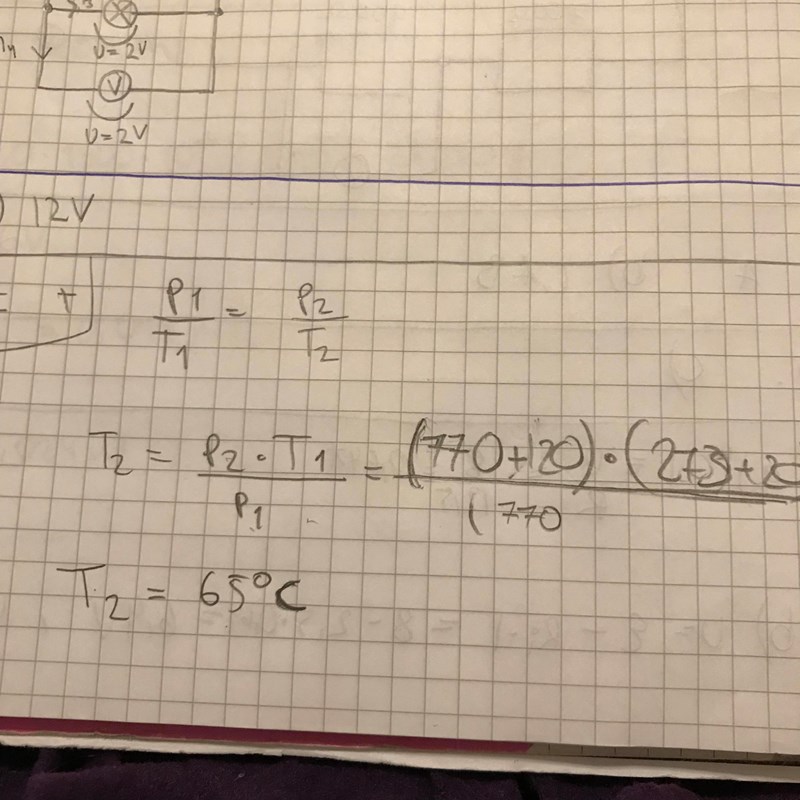Vid vilken temperatur antar kvicksilverytorna samma nivå? Ideala gaslagen.....
Hej, jag har följande fråga som jag försöker besvara men vet inte riktigt hur jag ska tänka. Jag tror att man ska använda sig av Ideala gaslagen men är inte helt säker :(
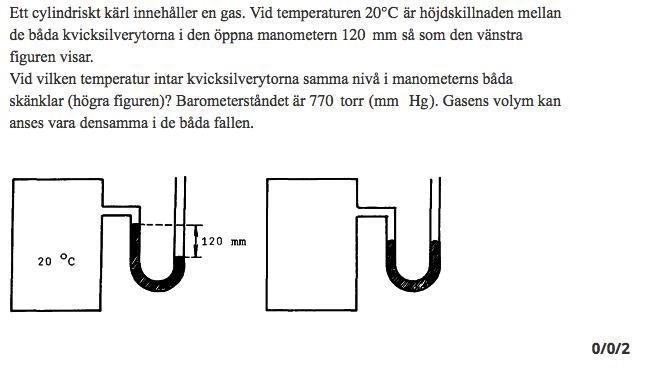
Om kvicksilverytorna är på samma höjd, innebär det att trycket inne i det cylindriska kärlet är lika stort som summan av det yttre lufttrycket och trycket från en 120 mm hög kvicksilverpelare.
Idealgaslagen säger att Pv = nRT. I det här fallet är v, n och R konstanta, så det gäller att där index 1 gäller vid temperaturen 20 C och index 2 gäller vid den högre temperaturen. I det här fallet blir det enklast att mäta trycket i enheten mmHg. Tänk på att man måste ange temperaturen i K.
Det stämmer att allmänna gaslagen ska användas. Kan du formulera i ord vad det är du behöver räkna ut? När du har gjort det kan du ställa upp ekvationer.
Jag tänkte precis som ni säger, men fick helt fel svar.
*lägger upp bild på hur jag tänkt om 5 sek*
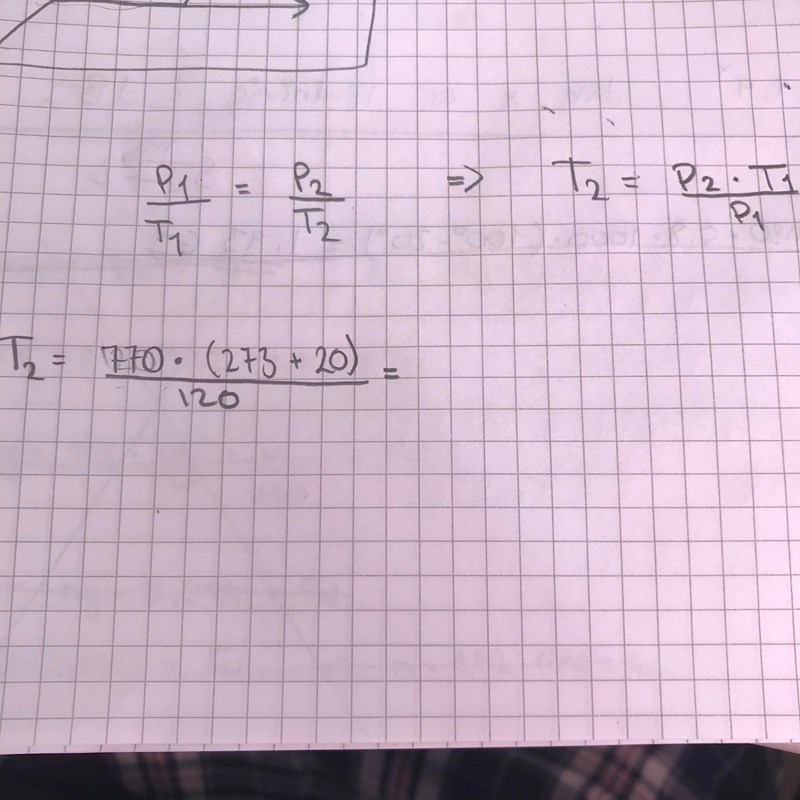
trycket inne i det cylindriska kärlet är lika stort som summan av det yttre lufttrycket och trycket från en 120 mm hög kvicksilverpelare
alltså inte bara 120.
Ska jag då dividera med
( 0,120 * 9,82 * 13 569 + 101 300 )?
Ibland är det enklare att inte använda SI-enheter.
Varför är P2 = 770 + 120 Pa?
Är det ursprungliga trycket 770? Hur kan man veta det?
Nej, jag tänkte fel. I den vänstra bilden är trycket på den högra kvicksilverytan 770 torr och trycket på den vänstra är 120 torr lägre. I den högra bilden är båda trycken lika, d v s 770 torr.
(1 torr = 1 mm Hg)
Det blir fortfarande fel temperatur :(
Visa hur du har gjort, annars kan vi inte hitta var det har blivt ifel!
I den vänstra bilden är trycket på den högra kvicksilverytan 770 torr och trycket på den vänstra är 120 torr lägre. I den högra bilden är båda trycken lika, d v s 770 torr.
I den vänstra bilden är alltså trycket i kolven 770-120 = 650 torr (och lufttrycket är 770 torr). Kvicksilverytan är ju högre upp på "kolv-sidan", så trycket måste vara lägre i kolven.
I den högra bilden är trycket i kolven lika med lufttrycket, d v s 770 torr.
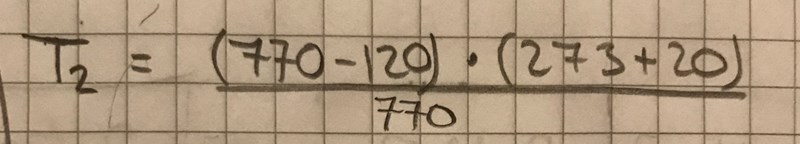
Blir det så?
Nej. Du har idealgaslagen . Vi är bara intresserade av p och V, så vi kan skriva om det till , där högerledet är konstant. Vi har alltså , vilket kan skrivas om till , alltså den högre temperaturen är lika med den lägre temperaturen multiplicerad med 770/650.
Det brukar vara en bra idé att behålla variablerna så länge som möjligt medan man förenklar, och inte sätta in siffrorna förrän på slutet.
Juste p2 var ju det högra med den okända temperaturen. Taaack då förstår jag :D