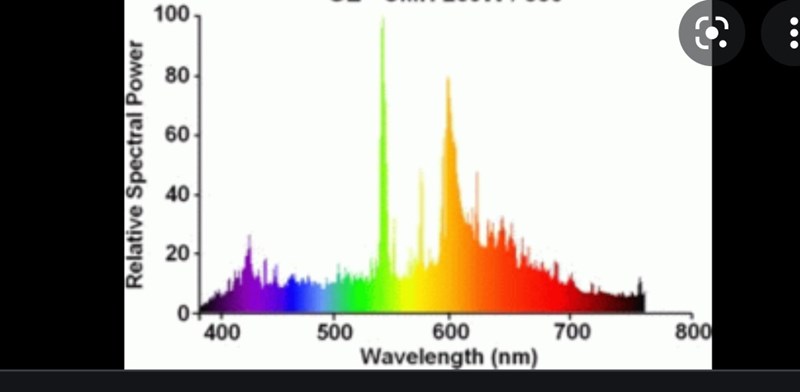
Vilka spektrum visar vilka lampa/ämne
Jag hade en fråga där det fanns tre bilder av emissionspektrum och man skulle avgöra vilka av emissionspektrum representerar vilka lampa. Jag kan inte hitta bilderna, men spektrallinjerna hade inga vågländer angivna, det enda informationen som angavs var bilderna av emissionspektrum. Hur kan man veta vilka emissionspektrum tillhör vilken ämne/lampa.
Jag tänkte på formeln 1/lamba =R( (1/m^2)- (1/n^2) ) alltså Rydberg formel. m och n är heltal som svarar mot ett spektralinje, men formeln funkar inte då först, så vet jag inte våglängd. Sedan vet jag inte vad R är eftersom jag tror den skiljer sig beroende på vilken atom man vill beräkna. och sist, jag vet inte hur jag kommer forsätta.
Jag tänkte sen på Bohrs postualt vilket är generellt och gäller för alla atomer ( hf=Wn -Wm där m och n är heltal och n är större än m). Men samma sak gällde här och jag vet inte hur jag ska använda den
Bilder av spektrum behövs.
Sedan kan man jämföra med tabeller eller med andra bilder.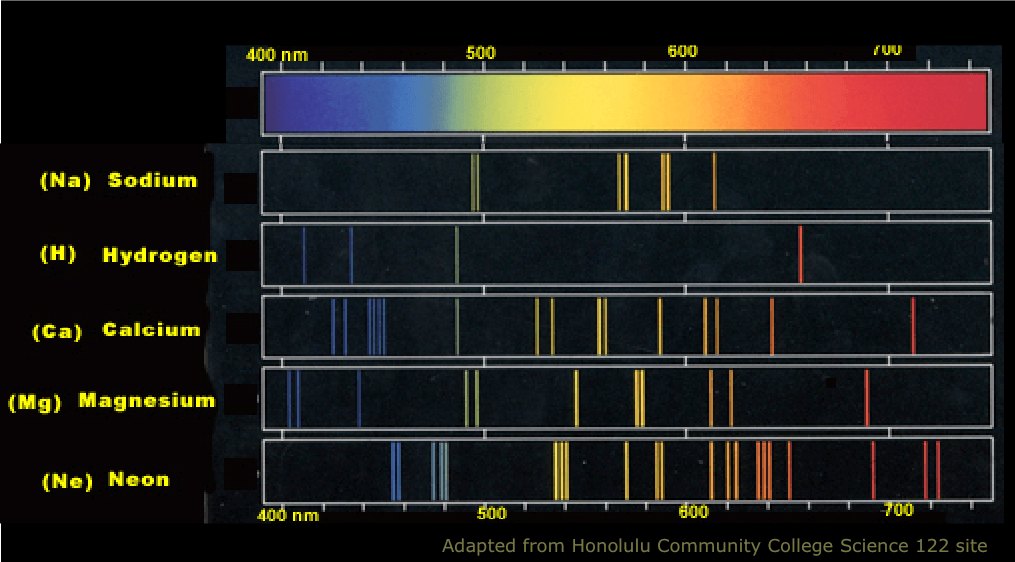
Har du inga våglängder så kan du ju inte göra några beräkningar och det var förmodligen en matchningsfråga som utgick från att du skulle ha någon slags faktakunskap så som att Neon har dominerande spektallinjer runt rött, att Natrium är associerat med gult, att ädelgaser med större atomtal ofta har fler spektrallinjer i det synliga spektrumet än ädelgaser med lägre atomtal, osv.
Man kan titta på Rydbergs formel och få en kvalitativ känsla för spektrallinjernas distribution (tunga vätelika ämnen har större effektiva konstanter R ~ R_H Z^2 (för vätelika ämnen) osv men i Fy2 skulle jag förvänta mig antingen att det var en faktafråga grundat i läsematerialet man fått eller att du missade något i frågan om vilken information du fått.
Pieter Kuiper skrev:Bilder av spektrum behövs.
Sedan kan man jämföra med tabeller eller med andra bilder.
ja, bilden såg ungefär så här förutom att det Stod inga namn på ämnen på sidan
Inlägg utflyttad från citatrutan då tråden annars blir svårare att följa. /Dracaena, moderator
SeriousCephalopod skrev:Har du inga våglängder så kan du ju inte göra några beräkningar och det var förmodligen en matchningsfråga som utgick från att du skulle ha någon slags faktakunskap så som att Neon har dominerande spektallinjer runt rött, att Natrium är associerat med gult, att ädelgaser med större atomtal ofta har fler spektrallinjer i det synliga spektrumet än ädelgaser med lägre atomtal, osv.
Man kan titta på Rydbergs formel och få en kvalitativ känsla för spektrallinjernas distribution (tunga vätelika ämnen har större effektiva konstanter R ~ R_H Z^2 (för vätelika ämnen) osv men i Fy2 skulle jag förvänta mig antingen att det var en faktafråga grundat i läsematerialet man fått eller att du missade något i frågan om vilken information du fått.
Men om man utgår ifrån den bilden ovanför går det inte att bestämma vad våglängden är ungefär? Och med det kan man göra någon beräkningar?
Var linjerna färgade på din bild? I så fall kan man få ett visst hum om våglängden hos de olika linjerna (eller om det stod att det var det synliga spektrumet som visades).
Smaragdalena skrev:Var linjerna färgade på din bild? I så fall kan man få ett visst hum om våglängden hos de olika linjerna (eller om det stod att det var det synliga spektrumet som visades).
Ja, de var färgad så jag skulle påstå att det borde vara i den synliga spektrum
men om man vet ungefär vad våglängden är, hur kan man beräkna?
Faattee skrev:hur kan man beräkna?
Det går inte med skolfysik.
Det finns program, till exempel ett gammalt program av Bob Cowan.
Men det går inte att säkert lita på resultaten, så man kollar alltid experimentella tabeller, "Moore's tables" av Charlotte Moore.
https://www.nist.gov/pml/atomic-spectra-database
Pieter Kuiper skrev:Faattee skrev:hur kan man beräkna?Det går inte med skolfysik.
Det finns program, till exempel ett gammalt program av Bob Cowan.
Men det går inte att säkert lita på resultaten, så man kollar alltid experimentella tabeller.
https://www.nist.gov/pml/atomic-spectra-database
Men emissionspektrumet fanns också sådant bilder, och jag börja tro att kanske det är en resonomang fråga. Men samtidigt var det inga matchningfråga.
Har dragit ut inlägget från citatet för att göra det enklare att följa tråden. /Dracaena, moderator
Där ser jag en grön linje. Då skulle jag kolla om resten av spektrumet stämmer med kvicksilver, som har en grön linje vid 546 nm.
Pieter Kuiper skrev:Där ser jag en grön linje. Då skulle jag kolla om resten av spektrumet stämmer med kvicksilver, som har en grön linje vid 546 nm.
så frågan är mer att man ska ha bra fakta om hur olika atomer ser ut för att kunna hitta svar?